
Wetenschap
Wat is het tegenovergestelde van zwavelzuur?
* chemische tegenstellingen: Het concept van een chemisch "tegenover" is lastig. We denken vaak aan tegenstellingen in termen van een spectrum (bijvoorbeeld warm/koud, licht/donker). Hoewel zwavelzuur een sterk zuur is, is er geen perfect overeenkomstige "tegengestelde" sterke basis.
* neutralisatie: Het dichtstbijzijnde concept van een tegenovergestelde is neutralisatie. Zwavelzuur (H₂so₄) is een sterk zuur. Om het te neutraliseren, zou u een sterke basis gebruiken zoals natriumhydroxide (NaOH). Deze reactie produceert zout (Na₂so₄) en water (H₂o), die beide neutraal zijn.
* functie: De belangrijkste functie van zwavelzuur is als een sterk zuur. Een "tegenovergestelde" kan een stof zijn met de primaire functie van een sterke basis zijn (zoals natriumhydroxide). Dit is echter geen echte chemische stof tegenover.
Dus samengevat: Er is niemand perfect tegenover zwavelzuur. Het dichtstbijzijnde concept is neutralisatie, waarbij een sterke basis wordt gebruikt om de zuurgraad tegen te gaan.
 Dreiging van droogte in de ontwikkelingslanden voor rijst en katoen in de EU intensiveert onderzoeksinspanningen
Dreiging van droogte in de ontwikkelingslanden voor rijst en katoen in de EU intensiveert onderzoeksinspanningen Hoe gedragen olifanten zich?
Hoe gedragen olifanten zich?  Hoe helpt culturele antropologie de wereld?
Hoe helpt culturele antropologie de wereld?  NASA's GPM toont regenval ten zuidoosten van de afgescheurde tropische cycloon Iris
NASA's GPM toont regenval ten zuidoosten van de afgescheurde tropische cycloon Iris Welke exotische soorten kunnen worden geïntroduceerd bij de aanleg van een golfbaan?
Welke exotische soorten kunnen worden geïntroduceerd bij de aanleg van een golfbaan?
Hoofdlijnen
- Hoe voelen ziekteverwekkers de omgeving? Wetenschappers identificeren de structuren van belangrijke eiwitten
- De kleinste krachten opsporen:hoe T-cellen indringers detecteren
- Wat is de microscopische ruimte die tussen zenuwcellen bestaat?
- Kunnen wetenschappers dinosaurussen klonen?
- Heeft volwassen rode bloedcellen chromosomen?
- Waarom krijgen demonen de schuld van slaapverlamming?
- Onthul de geheimen van plantgezondheid en koolstofopslag met rhizosphere-on-a-chip
- Hoe wordt het individu geproduceerd door aseksuele reproductie?
- Wat zijn enkele voorbeelden van homeostase in de huid?
- Houten bouwmaterialen brandwerend maken met een milieuvriendelijke coating

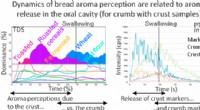
- Waarom een knapperige korst essentieel is voor het aroma en de smaak van baguettes
- Enzym kan een sleutelrol spelen bij het ontwerpen van medicijnen voor borstkanker en hersenaandoeningen

- Video:Hoe pittige peperhitte te verslaan (hint:melk is niet de beste)

- Machine learning-benadering kan helpen bij het ontwerpen van industriële processen voor de productie van geneesmiddelen

 Siliciumsandwiches voeden LHC's opgewaardeerde botsingslust
Siliciumsandwiches voeden LHC's opgewaardeerde botsingslust Kernreactoren met een nieuw voorgestelde barrière hadden Tsjernobyl en Fukushima kunnen weerstaan
Kernreactoren met een nieuw voorgestelde barrière hadden Tsjernobyl en Fukushima kunnen weerstaan Is kosmologie tegen het christelijke geloof?
Is kosmologie tegen het christelijke geloof?  Gezichtsherkenningsonderzoeker vecht Amazon tegen vooringenomen AI
Gezichtsherkenningsonderzoeker vecht Amazon tegen vooringenomen AI Vrouwelijke brandweerlieden kunnen de veiligheid verbeteren, maar afdelingscultuur moet veranderen
Vrouwelijke brandweerlieden kunnen de veiligheid verbeteren, maar afdelingscultuur moet veranderen De meest gedetailleerde radiokaart van de Melkweg
De meest gedetailleerde radiokaart van de Melkweg Dichter bij de aarde:een nieuwe techniek voor het onderzoeken van ultralage snelheidszones op de kern-mantelgrens van de aarde
Dichter bij de aarde:een nieuwe techniek voor het onderzoeken van ultralage snelheidszones op de kern-mantelgrens van de aarde  Wat zijn lithiumchloride en magnesiumhydroxide samengevoegd?
Wat zijn lithiumchloride en magnesiumhydroxide samengevoegd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

