
Wetenschap
Wat is de chemische vergelijking voor de bereiding van ammoniumbromide met behulp van kalium en sulfaat?
* kalium en sulfaat reageren niet om ammoniumbromide direct te vormen. Kalium (K) is een zeer reactief metaal en sulfaat (So₄²⁻) is een anion. Ze zouden reageren op het vormen van kaliumsulfaat (k₂so₄) en waarschijnlijk waterstofgas vrijgeven.
* ammoniumbromide vereist ammoniumionen (NH₄⁺). U hebt een bron van ammoniumionen nodig om ammoniumbromide te vormen.
Hier is hoe u ammoniumbromide kunt voorbereiden:
1. Begin met ammoniak (NH₃) en hydrobromzuur (HBR):
* NH₃ (G) + HBR (AQ) → NH₄BR (AQ)
2. Als alternatief kunt u ammoniumhydroxide (NH₄OH) reageren met hydrobromzuur (HBR):
* NH₄OH (AQ) + HBR (AQ) → NH₄BR (AQ) + H₂o (L)
Belangrijke opmerking: Deze reacties zijn in waterige oplossingen. U kunt vast ammoniumbromide verkrijgen door het water te verdampen.
U kunt kalium en sulfaat niet direct gebruiken om ammoniumbromide te bereiden. U hebt een bron van ammoniumionen (NH₄⁺) en bromide -ionen (Br⁻) nodig.
 Onderzoek laat zien hoe bioactieve stof belangrijke receptoren remt
Onderzoek laat zien hoe bioactieve stof belangrijke receptoren remt Hoe lachgas werkt
Hoe lachgas werkt  Welk element zou in combinatie met zwavel het liefst een ionische verbinding vormen?
Welk element zou in combinatie met zwavel het liefst een ionische verbinding vormen?  Voor waterstofenergie, alledaagse materialen zijn misschien bijna net zo goed als prijzig platina
Voor waterstofenergie, alledaagse materialen zijn misschien bijna net zo goed als prijzig platina Welke obligatie draagt elektronen over?
Welke obligatie draagt elektronen over?
Hoofdlijnen
- De sleutel tot het kweken van natuurlijk weefsel voor de reconstructie van het vrouwelijk voortplantingssysteem ontgrendeld
- Waarom zijn mannelijke spinnen klein, terwijl vrouwtjes gigantisch zijn?
- Wat is één cel verdeeld in twee identieke dochtercellen?
- Hoe een mRNA-sequentie
- Hoe wordt het organisme geclassificeerd?
- Wat zijn 4 manieren waarop micro -organismen het lichaam kunnen beschadigen?
- Gezond of ziek? Kleine celbelletjes kunnen het antwoord bevatten
- Wanneer een organisme zoals gist leeft door fermentatie, zet het pyrodruivenzuur uit glycolsis om in een andere samengestelde alcohol. Waarom direct uitscheiden?
- Gaan we het nu echt over walvissen hebben?
- Natuurkundigen krijgen nieuwe inzichten in nanosystemen met bolvormige opsluiting

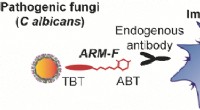
- Neutralisatie van pathogene schimmels met immunotherapeutica met kleine moleculen
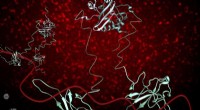
- Een diepe duik in het belangrijkste COVID-19-eiwit is een stap in de richting van nieuwe medicijnen, vaccins
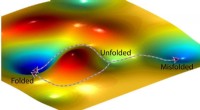
- Verborgen symmetrie gevonden in chemische kinetische vergelijkingen
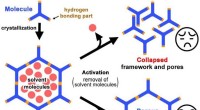
- Poreuze materialen werpen licht op milieuzuivering
 Leg de relatie uit tussen planten en een sfeer die geschikt is voor het in stand houden van het leven?
Leg de relatie uit tussen planten en een sfeer die geschikt is voor het in stand houden van het leven?  Wat voor soort wortel heeft een bonenplant?
Wat voor soort wortel heeft een bonenplant?  Waarom is de F/Cl-verhouding van de aarde niet chondritisch?
Waarom is de F/Cl-verhouding van de aarde niet chondritisch? Wat is de naam van een neuron dat neurale impuls overbrengt van sensorisch naar motorneuron?
Wat is de naam van een neuron dat neurale impuls overbrengt van sensorisch naar motorneuron?  Onderzoekers onderzoeken hoe de gevolgen van de droogte voor belangrijke voedselgewassen kunnen worden geminimaliseerd
Onderzoekers onderzoeken hoe de gevolgen van de droogte voor belangrijke voedselgewassen kunnen worden geminimaliseerd  Menigte die door muren telt, met wifi
Menigte die door muren telt, met wifi Wat zijn prisma's & piramides?
Wat zijn prisma's & piramides?  Onderzoek naar de link tussen buurten en scholen
Onderzoek naar de link tussen buurten en scholen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

