
Wetenschap
Kunnen waterstof en zuurstof een ionische binding vormen?
* elektronegativiteit: Zuurstof is veel elektronegatiefer dan waterstof. Dit betekent dat zuurstof een veel sterkere trek aan elektronen heeft. In een typische ionische binding neemt het ene atoom (het meer elektronegatieve) volledig een elektron van het andere atoom, waardoor tegengesteld geladen ionen ontstaan.
* de neiging van waterstof: Waterstof heeft slechts één proton en één elektron. Het heeft de neiging zijn elektron te verliezen en een positief geladen ion (H+) te worden in plaats van een elektron te krijgen om negatief geladen te worden.
wat er in plaats daarvan gebeurt:
Waterstof en zuurstof vormen een covalente binding waarin ze elektronen delen. Dit delen creëert een stabiel molecuul, water (h₂o).
Key Takeaway: Ionische bindingen treden meestal op tussen metalen en niet -metalen vanwege significante elektronegativiteitsverschillen.
 Hoe werkt een waterstofgenerator?
Hoe werkt een waterstofgenerator?  Wat is de formulesnaam voor NH4CL2?
Wat is de formulesnaam voor NH4CL2?  De mysteries van het leven oplossen:kristallografen identificeren 1, 000 eiwitstructuren
De mysteries van het leven oplossen:kristallografen identificeren 1, 000 eiwitstructuren Wat is de dampdruk voor water bij 100 ° C?
Wat is de dampdruk voor water bij 100 ° C?  Wetenschappers gebruiken röntgenstralen om de geheimen van schalie te kraken, een hoeksteen van een van de snelst groeiende energiebronnen van het land
Wetenschappers gebruiken röntgenstralen om de geheimen van schalie te kraken, een hoeksteen van een van de snelst groeiende energiebronnen van het land
 Kleine veranderingen kunnen grote besparingen opleveren in het watergebruik in de landbouw, zo blijkt uit onderzoek
Kleine veranderingen kunnen grote besparingen opleveren in het watergebruik in de landbouw, zo blijkt uit onderzoek  NASA ziet Atlantics Leslie een orkaan worden
NASA ziet Atlantics Leslie een orkaan worden Nieuwe studie helpt beleidsmakers de opwarming van de aarde tegen te gaan met technologie voor negatieve emissies
Nieuwe studie helpt beleidsmakers de opwarming van de aarde tegen te gaan met technologie voor negatieve emissies Welke term verwijst naar de niet-levende factoren van de omgeving?
Welke term verwijst naar de niet-levende factoren van de omgeving?  Meer huizen gebouwd in de buurt van wilde gebieden, wat leidt tot een groter risico op natuurbranden
Meer huizen gebouwd in de buurt van wilde gebieden, wat leidt tot een groter risico op natuurbranden
Hoofdlijnen
- Onderzoekers tonen aan dat een kankerafweermechanisme kan worden teruggedraaid om tumoren aan te vallen
- Wat is een accessoire -orgel voor het integumentaire systeem?
- Wat is het embryo -embryo van zaadspoornissen of een jonge plant?
- Kunnen data dolfijnen redden? Hoe wetenschappers NASA-gegevens gebruiken om het verband tussen zonnestormen en het stranden van dieren te bestuderen
- Uit onderzoek blijkt dat er minder schimmelgifstoffen aanwezig zijn in biologisch geteeld graan, vergeleken met conventioneel geteeld graan
- Twee jaar durend onderzoek toont aan dat sommige soorten eenjarige bloemen een plaats hebben in bestuivingsvriendelijke tuinen
- Hoeveel basenparen zijn er in wat als uw genoom?
- Onderwaterhitte inferno verwoest mediterrane koralen
- Welk molecuul is verantwoordelijk voor het transporteren van de genetische informatie gecodeerd op DNA van de kern naar het ribosoom?
- Studie onthult de ingewikkelde manier waarop twee eiwitten interageren om celbeweging te bevorderen, metastase
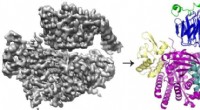
- Studie onthult de rol van platina bij de conversie van schone brandstof
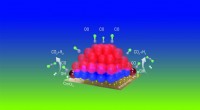
- Nieuwe doelstelling voor ontwikkeling van innovatieve antibiotica
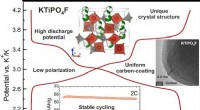
- Wetenschappers ontwikkelen nieuw kathodemateriaal voor metaal-ionbatterijen
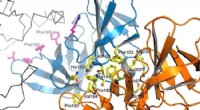
- Studie onthult details over hoe een veelgebruikte katalysator water splitst
 De PKA in titratie
De PKA in titratie Wat is de tak van de biologische wetenschap die bestudeert en beschrijft hoe lichaamsdelen werken of junctie?
Wat is de tak van de biologische wetenschap die bestudeert en beschrijft hoe lichaamsdelen werken of junctie?  Een samensmelting van microben:onderzoek toont aan dat omstandigheden met weinig voedingsstoffen de virale infectie veranderen
Een samensmelting van microben:onderzoek toont aan dat omstandigheden met weinig voedingsstoffen de virale infectie veranderen  Wat is de melkweg naast Melkweg?
Wat is de melkweg naast Melkweg?  Wetenschappers wijzen op een manier waarop nanodeeltjes immuuncellen beschadigen
Wetenschappers wijzen op een manier waarop nanodeeltjes immuuncellen beschadigen Waar begint de bron van rivier de Wolga?
Waar begint de bron van rivier de Wolga?  Tropische storm Irwins oostelijke kant bouwt voort op satellietbeelden
Tropische storm Irwins oostelijke kant bouwt voort op satellietbeelden SARS heeft de horeca niet voorbereid op de langdurige impact van COVID-19
SARS heeft de horeca niet voorbereid op de langdurige impact van COVID-19
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

