
Wetenschap
Een covalente verbinding wordt hoogstwaarschijnlijk gevormd?
Dit is waarom:
* Covalente binding omvat het delen van elektronen tussen atomen.
* niet -metalen Over het algemeen hebben een hoge elektronegativiteit (een neiging om elektronen aan te trekken).
* Wanneer niet -metalen binding, delen ze elektronen om een stabiele elektronenconfiguratie te bereiken, in plaats van elektronen over te dragen zoals bij ionische binding.
Voorbeelden van covalente verbindingen:
* Water (H₂o)
* Koolstofdioxide (co₂)
* Methaan (ch₄)
* Ethanol (c₂h₅oh)
Belangrijke opmerking: Hoewel niet -metalen typisch covalente verbindingen vormen, zijn er uitzonderingen, zoals waterstof (H) die covalente bindingen kunnen vormen met niet -metalen en ionische bindingen met metalen.
 Onderzoek onthult veelbelovende verschuivingen in vervuiling tijdens lockdown
Onderzoek onthult veelbelovende verschuivingen in vervuiling tijdens lockdown Chicago zou grenzen moeten stellen aan de uitstoot van broeikasgassen in gebouwen, aldus het rapport
Chicago zou grenzen moeten stellen aan de uitstoot van broeikasgassen in gebouwen, aldus het rapport  Verkeersverminderingen als gevolg van COVID-19 verbeteren de luchtkwaliteit in sommige staten, maar niet in alle
Verkeersverminderingen als gevolg van COVID-19 verbeteren de luchtkwaliteit in sommige staten, maar niet in alle Waar kunt u een lijst met vriendelijke woorden vinden om de aarde te beschrijven?
Waar kunt u een lijst met vriendelijke woorden vinden om de aarde te beschrijven?  Zal graslandbodem een verandering doorstaan?
Zal graslandbodem een verandering doorstaan?
Hoofdlijnen
- Welke combinatie van chromosomen resulteert in een jongen?
- Zijn dierlijke cellen en planten dezelfde grootte?
- Noordse veelvraten hebben de slechtste status op het gebied van genetische diversiteit, blijkt uit uitgebreide Euraziatische onderzoeken
- Wat zijn de aanpassingen van bladepidermale cellen?
- De meeste exemplaren van schadelijke recessieve allelen worden gedragen?
- Nieuwe formule voorspelt hoe mensen de komende decennia zullen migreren
- Wat zijn de vier weefselsoorten van het menselijk lichaam?
- Een ongewoon wezen ontwaakt uit de winterslaap. Dit is waarom wetenschappers enthousiast zijn.
- Wat is een niet -Medelische eigenschap?
- Kleine elektrische velden kunnen een beslissende rol spelen bij de vorming van diamant

- Nieuw materiaal kan helpen de batterijkosten voor elektrische auto's te verlagen, telefoons
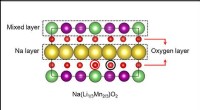
- Omhulsels drijven krachtige nieuwe kunstmatige spieren aan

- Krachtige antimicrobiële gevonden die veelbelovend is in het bestrijden van stafylokokbesmettingen

- Onderzoekers stellen een strategie voor voor katalytische regiodivergente hydrosilylering van isopreen
 Waarom vormen edelen gassen geen bindingen met andere elementen?
Waarom vormen edelen gassen geen bindingen met andere elementen?  Hoe een stalen I-balken te berekenen Gewicht
Hoe een stalen I-balken te berekenen Gewicht  Hoe kunt u zowel de woorden die deze verbijsterd zijn als Bbejeebers in dezelfde zin gebruiken?
Hoe kunt u zowel de woorden die deze verbijsterd zijn als Bbejeebers in dezelfde zin gebruiken?  Wat zijn de overeenkomsten tussen eierdoppen en tanden?
Wat zijn de overeenkomsten tussen eierdoppen en tanden?  Waar vindt u fossielen?
Waar vindt u fossielen?  Wat is de verhoging van de regio Great Plains?
Wat is de verhoging van de regio Great Plains?  Wie is slimmer in de klas:mannen of vrouwen? Nieuw onderzoek toont aan dat het allemaal om perceptie draait
Wie is slimmer in de klas:mannen of vrouwen? Nieuw onderzoek toont aan dat het allemaal om perceptie draait  Hoeveel atomen in HNO3?
Hoeveel atomen in HNO3?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

