
Wetenschap
Als een mengsel van twee gassen totale druk 5,7 atm heeft. één gas gedeeltelijk 4.1 atm Wat is het andere gas?
Dalton's wet van gedeeltelijke druk
De wet van Dalton stelt dat de totale druk van een mengsel van gassen gelijk is aan de som van de gedeeltelijke druk van de afzonderlijke gassen.
formule:
P totaal =P 1 + P 2 + ... + p n
Waar:
* P totaal is de totale druk van het mengsel
* P 1 , P 2 , ... p n zijn de gedeeltelijke druk van elk individueel gas
Berekening:
1. Identificeer de bekende waarden:
* P totaal =5,7 atm
* P 1 =4.1 atm (gedeeltelijke druk van één gas)
2. Laat p 2 vertegenwoordigen de gedeeltelijke druk van het andere gas.
3. Pas de wet van Dalton toe:
5.7 ATM =4.1 ATM + P 2
4. Oplossen voor p 2 :
P 2 =5,7 ATM - 4.1 ATM =1,6 ATM
Antwoord: De gedeeltelijke druk van het andere gas is 1,6 atm.
 Haat-liefdeverhouding tussen oplosmiddel en water leidt tot een betere afbraak van biomassa
Haat-liefdeverhouding tussen oplosmiddel en water leidt tot een betere afbraak van biomassa Wat de elektronenconfiguratie van calcium in lange vorm?
Wat de elektronenconfiguratie van calcium in lange vorm?  Hoe bereken je het aantal gram Al in 286 g Al2O3.?
Hoe bereken je het aantal gram Al in 286 g Al2O3.?  Het decoderen van het flavonoïdemetabolisme:een nadere blik op plantaardige diëten
Het decoderen van het flavonoïdemetabolisme:een nadere blik op plantaardige diëten  Wat is de elektronenpuntstructuur gevormd tussen calcium en chloor?
Wat is de elektronenpuntstructuur gevormd tussen calcium en chloor?
Hoofdlijnen
- Wat zijn de 6 biomen van de wereld?
- Hoe verschillen het zenuwstelsel en het endocriene systeem?
- Heeft iemand artikelen gepubliceerd met Advances in Microbiology? Ik werd voorgesteld om mijn eigen artikel daarin in te dienen. Wie kan het mij vertellen?
- Welke term wordt gebruikt voor een plant die zaad produceert met beschermende dekking?
- Drie nieuwe soorten grondslangen ontdekt onder kerkhoven en kerken in Ecuador
- Welke bacteriën voeren de gisting van een glucosemolecuul uit?
- Wat zijn de drie belangrijkste wetenschapsgroepen?
- Is een eiwit lipide -eiwit of geen van beide?
- Hoe chromosomen uit DNA te maken
- Orde brengen in chaotische bubbels kan mijnbouw duurzamer maken

- Elektromagnetische stralingsbeschermingsschermen ontwikkeld

- Glycerolfosfaat dient als een terminator van glycaanverlenging bij kanker maligniteiten

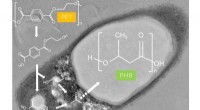
- Hoe een bacterie de plasticvervuilingscrisis kan helpen oplossen
- Nooit eerder geziene glasschade op nanoniveau zien

 Theorie geeft transparantie over hoe glas breekt
Theorie geeft transparantie over hoe glas breekt  Naam 4 Planeten dat astronomen positief zijn, hebben er ringen om hen heen?
Naam 4 Planeten dat astronomen positief zijn, hebben er ringen om hen heen?  Vernieuwd MIT Climate Portal heeft tot doel het publiek te informeren en te machtigen
Vernieuwd MIT Climate Portal heeft tot doel het publiek te informeren en te machtigen Peter Higgs transformeerde wat we weten over de bouwstenen van het universum
Peter Higgs transformeerde wat we weten over de bouwstenen van het universum  Wat zijn de 4 belangrijkste bodemlagen?
Wat zijn de 4 belangrijkste bodemlagen?  Kan een rots tegelijkertijd door verwering en erosie gaan?
Kan een rots tegelijkertijd door verwering en erosie gaan?  Typen verwarmingsapparaten voor gebruik in wetenschappelijke experimenten
Typen verwarmingsapparaten voor gebruik in wetenschappelijke experimenten Wat is het verschil tussen colloïde oplossing voor mengsel?
Wat is het verschil tussen colloïde oplossing voor mengsel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

