
Wetenschap
De elementen in het periodiek systeem met een volledig gevulde buitenafschil staan bekend als?
De elementen in het periodiek systeem met een volledig gevulde buitenste subschaal staan bekend als nobele gassen .
Dit is waarom:
* buitenste elektronenconfiguratie: Nobele gassen hebben een volledige buitenste elektronenschil (of valentieschaal). Dit betekent dat ze een stabiele elektronenconfiguratie hebben, waardoor ze zeer niet -reactief zijn.
* Inerte gassen: Vanwege hun stabiele configuratie worden ze vaak "inerte gassen" genoemd omdat ze niet gemakkelijk chemische bindingen vormen met andere elementen.
Voorbeelden van edelgassen:
* Helium (hij)
* Neon (ne)
* Argon (AR)
* Krypton (KR)
* Xenon (XE)
* Radon (RN)
 Kan een verbinding in zijn samenstellende elementen worden gescheiden?
Kan een verbinding in zijn samenstellende elementen worden gescheiden?  Wat is titaniumdioxide pH?
Wat is titaniumdioxide pH?  Inzetstuk voor gezichtsmaskers kan helpen bij het diagnosticeren van ziektetoestanden, studie toont
Inzetstuk voor gezichtsmaskers kan helpen bij het diagnosticeren van ziektetoestanden, studie toont Wat is de chemische formule voor kalium heptaoxodichromate vi?
Wat is de chemische formule voor kalium heptaoxodichromate vi?  Waarom kan magnesium reageren met CO2, maar niet met goud?
Waarom kan magnesium reageren met CO2, maar niet met goud?
 Nieuw bewijs toont aan dat beplanting rond schoolpleinen kinderen beschermt tegen luchtvervuiling
Nieuw bewijs toont aan dat beplanting rond schoolpleinen kinderen beschermt tegen luchtvervuiling Lorena komt aan land in het zuidwesten van Mexico als orkaan van categorie 1
Lorena komt aan land in het zuidwesten van Mexico als orkaan van categorie 1 Tekenen van eerdere mega-bevingen in Californië tonen het gevaar van de Big One op San Andreas Fault
Tekenen van eerdere mega-bevingen in Californië tonen het gevaar van de Big One op San Andreas Fault Wat deden de Indianen in de wetenschap?
Wat deden de Indianen in de wetenschap?  aardbeving met een kracht van 6,3 op de schaal van Richter ten zuiden van Bali in Indonesië
aardbeving met een kracht van 6,3 op de schaal van Richter ten zuiden van Bali in Indonesië
Hoofdlijnen
- Onderzoekers leveren bewijs van hoe eiwitten vouwen
- Het simuleren van seks met walvisachtigen met kadaverdelen biedt inzicht in mariene copulatie
- Wat is een andere naam voor een gewone microscoop?
- Wat is een organisme dat in een gastheercel leeft?
- MATE-transporter vergemakkelijkt het transport van bitter saponine van cytoplasma naar vacuole
- Hoe schizofrenie werkt
- Een middel om vrij grote deeltjes in de cel te brengen?
- Welke structuren worden voornamelijk gevonden in de Palisade -laag van Mesophyll?
- Wat is een neerslag in de wetenschap?
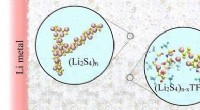
- Optimalisatie van de elektrolyten van lithium-zwavelbatterijen voor een lange levensduur
- Plunger, espresso, filter? Alleen omdat je koffie bitter is, wil nog niet zeggen dat hij sterker is

- Wetenschappers creëren een nieuw type intelligent materiaal

- Onderzoekers maken fotonische materialen voor krachtig, efficiënt op licht gebaseerd computergebruik

- Team ontwikkelt snelle authenticatiemethode voor Chinese medicijnen

 Onderzoekers optimaliseren grafeen voor verschillende toepassingen
Onderzoekers optimaliseren grafeen voor verschillende toepassingen Wat zijn verbindingen tussen atomen?
Wat zijn verbindingen tussen atomen?  Hoe konden wetenschappers en astronauten de kenmerken van de maan testen?
Hoe konden wetenschappers en astronauten de kenmerken van de maan testen?  Voorbij de wolken:sterrenstelsels achter sterrenstelsels vinden
Voorbij de wolken:sterrenstelsels achter sterrenstelsels vinden Welke maand zie je het sterrenbeeld Delphinus?
Welke maand zie je het sterrenbeeld Delphinus?  Airbnb biedt huisvesting aan 100, 000 crisishulpverleners
Airbnb biedt huisvesting aan 100, 000 crisishulpverleners Hoe NASA's Romeinse telescoop de leeftijd van sterren zal meten
Hoe NASA's Romeinse telescoop de leeftijd van sterren zal meten  Hoe kan het kookpunt worden gebruikt om erachter te komen of een stof puur is?
Hoe kan het kookpunt worden gebruikt om erachter te komen of een stof puur is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

