
Wetenschap
Hoe noem je binaire ionische verbinding?
stappen
1. Identificeer het metaal (kation): Het metaal is het positief geladen ion.
2. Identificeer het niet -metaal (anion): Het niet -metaal is het negatief geladen ion.
3. Noem het metaal: Gebruik de naam van het metaal zoals het op het periodiek systeem wordt weergegeven.
4. Noem het niet -metaal: Wijzig het einde van de naam van de niet-metalen in "-ide".
* Voorbeeld:zuurstof wordt "oxide", chloor wordt "chloride", stikstof wordt "nitride".
5. Combineer de namen: Schrijf eerst de metalen naam, gevolgd door de niet-metalen naam met het einde "-ide".
Voorbeeld:NaCl
* metaal: Natrium (NA)
* niet -metaal: Chloor (CL)
* naam: Natriumchloride
Dingen om in gedachten te houden:
* overgangsmetalen: Overgangsmetalen kunnen meerdere positieve ladingen vormen. Om de lading aan te geven, gebruik Romeinse cijfers tussen haakjes na de metalen naam.
* Voorbeeld:FECL2 is ijzer (ii) chloride, fecl3 is ijzer (iii) chloride
* Polyatomische ionen: Dit zijn ionen die meer dan één atoom bevatten. Je moet hun namen en kosten kennen om de naam van de compound te schrijven.
* Voorbeeld:Na2SO4 is natriumsulfaat (sulfaat is SO4 met een -2 lading)
Laten we oefenen met een ander voorbeeld:
K2O
* metaal: Kalium (k)
* niet -metaal: Zuurstof (O)
* naam: Kaliumoxide
Key Points
* Binaire ionische verbindingen zijn altijd neutraal. De positieve lading van het metaalkation moet de negatieve lading van het niet -metaalanion in evenwicht brengen.
* Romeinse cijfers worden alleen gebruikt wanneer het metaal meer dan één lading kan hebben.
* U kunt een periodieke tabel gebruiken om u te helpen metalen en niet -metalen te identificeren.
Laat het me weten als je nog meer voorbeelden wilt proberen!
 Vier basiscomponenten van een ecosysteem
Vier basiscomponenten van een ecosysteem  Eco-zoekmachine ziet toename van downloads terwijl Amazon brandt
Eco-zoekmachine ziet toename van downloads terwijl Amazon brandt Is de consequentialistische ethiek belangrijk in het behoud en is het een essentiële componenten de biodiversiteit?
Is de consequentialistische ethiek belangrijk in het behoud en is het een essentiële componenten de biodiversiteit?  NASA ziet subtropische storm 11S nog steeds wervelen
NASA ziet subtropische storm 11S nog steeds wervelen Meer flexibiliteit voor telers nodig tijdens droogte
Meer flexibiliteit voor telers nodig tijdens droogte
Hoofdlijnen
- Welke functie heeft emb-agar?
- Hoe menselijk sperma echt zwemt:nieuw onderzoek daagt eeuwenoude veronderstellingen uit
- Welke tak van de geneeskunde richt zich op de studietumoren en kanker?
- Wat zijn twee soorten informatie die wetenschappers proberen af te leiden uit de studiefossielen?
- Wetenschappers vinden ontbrekende schakel om te begrijpen hoe planten vitamine C aanmaken
- Wat is de een gevolgtrekking?
- Eicellen en zaadcellen worden geproduceerd in?
- Hebben vissen last van zuurstofgebrek?
- Nieuwe soorten ontdekt in Maleisisch regenwoud tijdens ongekende, onderzoek van boven naar beneden
- De wetenschap van geur bevorderen - met een vleugje musk

- Onderzoekers stellen nieuwe koppelingsstrategie voor organische afvalwaterzuivering voor

- Onderzoekers verbeteren de synthese van bismutwolframaat met een milieuvriendelijke procedure
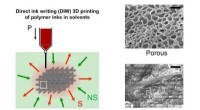
- Onderzoekers ontwikkelen een unieke methode om 3D poreuze structuren te fabriceren
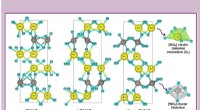
- Hoe metaalatomen zich kunnen rangschikken op een isolator

 Welke is warmer 1C of 69F?
Welke is warmer 1C of 69F?  NASA-stagiairs helpen het terminatorprobleem op te lossen via GLOBE challenge
NASA-stagiairs helpen het terminatorprobleem op te lossen via GLOBE challenge Waar is achohol van gemaakt?
Waar is achohol van gemaakt?  Wat is kwantumvreemdheid?
Wat is kwantumvreemdheid?  Fijnstofvervuiling:kunnen we microsensormetingen vertrouwen?
Fijnstofvervuiling:kunnen we microsensormetingen vertrouwen? Hoe het magnetisch veld van een permanente magneet uit te schakelen
Hoe het magnetisch veld van een permanente magneet uit te schakelen Wanneer werd Apollo 11 gebouwd?
Wanneer werd Apollo 11 gebouwd?  Werknemers een stem geven verbetert de retentie
Werknemers een stem geven verbetert de retentie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

