
Wetenschap
Wat is sterker hydroastatisch zuur of fluoroantimonzuur?
fluoroantimonzuur wordt beschouwd als de sterkste Superacid Bekend, met een geschatte hammett -zuurgraadfunctie (H0) van -31.3. Dit betekent dat het meer dan 10^16 keer sterker is dan geconcentreerd zwavelzuur.
hydrofluorzuur is een zwak zuur met een H0 van ongeveer 3,15.
Dit is de reden waarom fluoroantimonzuur zoveel sterker is:
* zeer reactief: Fluoroantimonzuur wordt gevormd door het mengen van waterstoffluoride (HF) en antimoon pentafluoride (SBF5). De reactie vormt een zeer reactieve soort die gemakkelijk protonen (H+) kan doneren.
* Hoog ionisatiepotentieel: De fluoride -ionen in fluoroantimonzuur zijn zeer elektronegatief, wat een sterke positieve lading op de waterstofatomen creëert, waardoor ze zeer zuur zijn.
* stabilisatie van de conjugaatbasis: De conjugaatbasis van fluoroantimonzuur (SBF6-) wordt sterk gestabiliseerd door de sterke elektronegatieve fluoratomen, wat verder bijdraagt aan de sterkte van het zuur.
Hydrofluorzuur is daarentegen een zwak zuur omdat de waterstof-fluorinebinding relatief sterk is, waardoor het moeilijk is om een proton te doneren.
Daarom is fluoroantimonzuur enorm sterker dan hydrofluorinezuur.
 Hoe noemde Robert Boyle de groepen atomen die hij bestudeerde?
Hoe noemde Robert Boyle de groepen atomen die hij bestudeerde?  Duurzame nylonproductie mogelijk gemaakt door ontdekking van bacteriën
Duurzame nylonproductie mogelijk gemaakt door ontdekking van bacteriën Wat is de massa HCl die nodig is om volledig te reageren met 5,2 gram Mg?
Wat is de massa HCl die nodig is om volledig te reageren met 5,2 gram Mg?  Organische zonnecellen die 10 jaar meegaan in de ruimte
Organische zonnecellen die 10 jaar meegaan in de ruimte Meringue-achtig materiaal kan vliegtuigen zo stil maken als een haardroger
Meringue-achtig materiaal kan vliegtuigen zo stil maken als een haardroger
 Onderzoeker onderzoekt mogelijke link tussen klimaatverandering en watertoxiciteit
Onderzoeker onderzoekt mogelijke link tussen klimaatverandering en watertoxiciteit Wat zijn de factoren die de zwaartekracht beïnvloeden?
Wat zijn de factoren die de zwaartekracht beïnvloeden?  Antarctische ijskloof verspreidt zich:nieuwe tak onthuld in de nieuwste gegevens van ijsplaat
Antarctische ijskloof verspreidt zich:nieuwe tak onthuld in de nieuwste gegevens van ijsplaat Warren Buffett zegt dat steenkool geen comeback zal maken
Warren Buffett zegt dat steenkool geen comeback zal maken Maak je eigen broeikasgaslogger
Maak je eigen broeikasgaslogger
Hoofdlijnen
- Antwoord Welk orgel wordt zowel uit het weefsel van het embryo als de moeder gemaakt?
- Wat is het bijproduct van cellulaire ademhaling dat BTB geel verandert?
- Waarom is osmose belangrijk in uw lichaamscellen?
- Chimpansees in gevangenschap vertonen tekenen van een aangetaste geestelijke gezondheid
- De vroegste landdieren hadden minder schedelbotten dan vissen, waardoor hun evolutie werd beperkt
- Wat is de besmetting afgewezen bij omgekeerde osmose?
- Waarom is het skeletstelsel belangrijk?
- Biofysici onthullen hoe drie eiwitten samenwerken om de cellulaire beweging te verfijnen
- Hoe verschilt het ene eiwit van een ander eiwit?
- Onderzoekers onthullen robuuste ethaan-vangende poreuze organische kooi voor efficiënte ethyleenzuiveringstoepassing

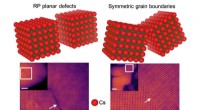
- Wanneer een defect gunstig kan zijn
- Chemici ontwikkelen nieuwe technologie om te voorkomen dat lithium-ionbatterijen vlam vatten

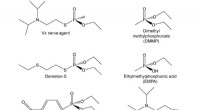
- Eiwit dat chemische oorlogsvoering kan voorkomen, gemaakt
- Een nieuw ontwerp voor flowbatterijen

 Zijn vitamines natuurlijke stoffen uit de aardkorst?
Zijn vitamines natuurlijke stoffen uit de aardkorst?  Afvalwater bevat voedingsstoffen, energie en edele metalen - wetenschappers leren hoe ze deze kunnen terugwinnen
Afvalwater bevat voedingsstoffen, energie en edele metalen - wetenschappers leren hoe ze deze kunnen terugwinnen Taalvaardigheden zijn van cruciaal belang voor het begrijpen van residentiële segregatie, zegt onderzoek
Taalvaardigheden zijn van cruciaal belang voor het begrijpen van residentiële segregatie, zegt onderzoek  Door klimaat beïnvloede veranderingen in bloei, vruchtvorming heeft ook invloed op de vogelstand, activiteiten
Door klimaat beïnvloede veranderingen in bloei, vruchtvorming heeft ook invloed op de vogelstand, activiteiten Opgraving Pompeii onthult Narcissus-fresco in oud atrium
Opgraving Pompeii onthult Narcissus-fresco in oud atrium Versierde nanodeeltjes voorkomen anafylaxie zonder bijwerkingen te veroorzaken in muisstudie
Versierde nanodeeltjes voorkomen anafylaxie zonder bijwerkingen te veroorzaken in muisstudie  Drones trainen om bronnen van broeikasgassen te detecteren
Drones trainen om bronnen van broeikasgassen te detecteren  Welk kenmerk is afkomstig waar de watertafel het landoppervlak kruist?
Welk kenmerk is afkomstig waar de watertafel het landoppervlak kruist?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

