
Wetenschap
Wat is de Lewis -structuur van CL2O7?
1. Bereken het totale aantal valentie -elektronen:
* Chloor (CL) heeft 7 valentie -elektronen en er zijn twee CL -atomen:7 * 2 =14 elektronen
* Zuurstof (O) heeft 6 valentie -elektronen en er zijn zeven O -atomen:6 * 7 =42 elektronen
* Totale valentie -elektronen:14 + 42 =56 elektronen
2. Bepaal het centrale atoom:
* Zuurstof is elektronegatiefer dan chloor, dus het zal het centrale atoom zijn.
3. Verbind de atomen met enkele bindingen:
* Schik de zeven zuurstofatomen rond het centrale zuurstofatoom.
* Elk zuurstofatoom vormt een enkele binding met het centrale zuurstofatoom.
4. Verdeel de resterende elektronen als eenzame paren:
* Elk zuurstofatoom heeft twee eenzame paren nodig om zijn octet te voltooien.
* Het centrale zuurstofatoom heeft twee enige paren nodig om zijn octet te voltooien.
5. Controleer op formele kosten:
* De formele lading van een atoom wordt berekend als:(valentie -elektronen) - (niet -bindende elektronen) - (1/2 * bindingselektronen)
* De formele ladingen moeten worden geminimaliseerd om een stabiele structuur te bereiken.
6. Overweeg meerdere bindingen:
* Om formele ladingen te minimaliseren, moeten we dubbele bindingen toevoegen tussen sommige zuurstofatomen en het centrale zuurstofatoom.
* De uiteindelijke structuur zal drie dubbele bindingen hebben, met de andere vier oxygens met een enkele gebonden aan de centrale zuurstof.
De laatste Lewis -structuur van Cl₂o₇:
`` `
O
/ \
Cl o
/ \ / \
O O O
/ \ / \ / \
Cl o o o
`` `
Sleutelpunten:
* Elk chlooratoom is verbonden met twee zuurstofatomen, met één dubbele binding en één enkele binding.
* Het centrale zuurstofatoom heeft drie dubbele bindingen en twee eenzame paren.
* Alle atomen hebben een compleet octet van elektronen.
Opmerking: Er zijn resonantiestructuren voor Cl₂o₇, waar de dubbele bindingen kunnen verschuiven. De hierboven getoonde structuur is echter de meest voorkomende en stabiele weergave.
Hoofdlijnen
- Witte bloedcellen vormen de basis van welk systeem in lichaam?
- Forsyth-wetenschappers krijgen meer inzicht in hoe embryo's zich onderscheiden van links en rechts
- Maagdelijke geboorten door parthenogenese:hoe vrouwtjes sommige soorten zich kunnen voortplanten zonder mannetjes
- De enige essentiële organel van een cel?
- Welke voedingsstoffen zijn alle organismen nodig?
- Hoe vergeten soorten twee keer uitsterven
- Hoe is celdeling vergelijkbaar met je levenscyclus?
- Hoe behoudt de afwisseling van meiose en bemesting in levenscycli die seksueel reproducerende organismen voor elke soort normaal chromosoomtelling behouden?
- Waarom wordt wetenschap de naam Wetenschap genoemd?
- Ontdekking van hoe mensen de geur van de dood ervaren, kan levens redden

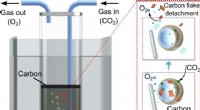
- Vloeibaar metaal bewezen goedkope en efficiënte CO2-converter
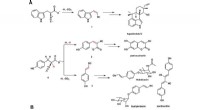
- Onderzoekers onderzoeken enzymen die een kation gebruiken, geen zuurstoftoevoeging, om reacties te stimuleren
- Vallen voor energiebronmoleculen in cellen
- Watermoleculen uit elkaar halen om schone brandstof te genereren:onderzoek naar een veelbelovend materiaal

 Waarom is een lege shampoofles zo gemakkelijk om te gooien?
Waarom is een lege shampoofles zo gemakkelijk om te gooien? Bosbranden in mediterrane bossen aanpakken
Bosbranden in mediterrane bossen aanpakken Asteroïde, klimaatverandering niet verantwoordelijk voor massale uitsterving 215 miljoen jaar geleden
Asteroïde, klimaatverandering niet verantwoordelijk voor massale uitsterving 215 miljoen jaar geleden Waarom is de revolutie van Jupiters period?
Waarom is de revolutie van Jupiters period?  Criteria voor de vermindering van de milieu-impact toegepast in het Romeinse theater van Italica
Criteria voor de vermindering van de milieu-impact toegepast in het Romeinse theater van Italica Four Corners dwangarbeid exposé laat zien waarom je misschien door slaven gemaakte kleding draagt
Four Corners dwangarbeid exposé laat zien waarom je misschien door slaven gemaakte kleding draagt Wat zijn de fasen van natuurlijke selectie?
Wat zijn de fasen van natuurlijke selectie?  De componenten van een mengsel worden meestal efficiënt van elkaar gescheiden op basis van hun?
De componenten van een mengsel worden meestal efficiënt van elkaar gescheiden op basis van hun?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


