
Wetenschap
Is Diamond een geleider of isolator?
Dit is waarom:
* binding: Diamond heeft een zeer sterke covalente bindingsstructuur. Elk koolstofatoom is strak gebonden aan vier andere koolstofatomen en vormt een rigide rooster.
* Elektronenmobiliteit: De elektronen in de covalente bindingen worden strak vastgehouden en kunnen niet vrij bewegen. Dit betekent dat ze niet gemakkelijk een elektrische stroom kunnen dragen.
* Band Gap: Diamond heeft een zeer grote bandspleet, wat betekent dat veel energie nodig is om een elektron op een geleidingsband te opwinden en een stroom te laten dragen.
Er zijn echter enkele uitzonderingen:
* Hogedruk diamant: Onder extreem hoge druk kan Diamond een geleider worden. Dit komt omdat de druk de elektronische structuur van het materiaal kan veranderen.
* gedoteerde diamant: Onzuiverheden (zoals boor of fosfor) kunnen aan Diamond worden toegevoegd om het semi-geleidend te maken. Dit proces wordt doping genoemd.
Over het algemeen wordt Diamond echter beschouwd als een zeer goede isolator in zijn natuurlijke vorm.
 Easy Science Project Ideeën voor de 7e Grade
Easy Science Project Ideeën voor de 7e Grade Wetenschappers gebruiken trechtervisie om goedkope en efficiënte zonne-energie te pionieren
Wetenschappers gebruiken trechtervisie om goedkope en efficiënte zonne-energie te pionieren Wat voor soort reactie vindt plaats als zetmeelmoleculen worden omgezet in het verminderen van suikers?
Wat voor soort reactie vindt plaats als zetmeelmoleculen worden omgezet in het verminderen van suikers?  Een radicale benadering van methaanoxidatie tot methanol
Een radicale benadering van methaanoxidatie tot methanol Hoeveel elektronen zullen fluor delen om covalente bindingen te laten voltooien zijn buitenste energieniveau?
Hoeveel elektronen zullen fluor delen om covalente bindingen te laten voltooien zijn buitenste energieniveau?
 Microplasticvervuiling wijdverbreid in Britse meren en rivieren, studie toont
Microplasticvervuiling wijdverbreid in Britse meren en rivieren, studie toont Hoe Honey Bee te maken Feromonen
Hoe Honey Bee te maken Feromonen Onderzoekers tonen aan dat de mug een gastheer ruikt voordat hij deze ziet
Onderzoekers tonen aan dat de mug een gastheer ruikt voordat hij deze ziet  Het voorspellen van droogte in het Amerikaanse Westen is nu nog moeilijker geworden
Het voorspellen van droogte in het Amerikaanse Westen is nu nog moeilijker geworden Rubber in het milieu:waar het loopvlak van onze banden naar toe verdwijnt
Rubber in het milieu:waar het loopvlak van onze banden naar toe verdwijnt
Hoofdlijnen
- Het effect van temperatuur op celmembranen
- Onderzoek toont aan hoe genactie kan leiden tot diabetespreventie en -genezing
- Wat is de Thermosophere -laag?
- Wat is celfusie?
- Door zich te hechten aan het lichaam van een walvisjucca -motten kunnen worden voeden terwijl ze door voedingsrijk rijk water waar of onwaar beweegt?
- Wat is het embryo -embryo van zaadspoornissen of een jonge plant?
- Wat dienen als enzymen koolhydraten lipiden lipiden nucleïnezuren eiwitten?
- Waar komen de allelen voor een eigenschap in een zygote vandaan?
- Hoe zou wetenschapper gegevens organiseren die zijn verzameld uit een experiment in een grafiek?
- Mysterieuze cellulaire druppeltjes komen in beeld
- Hoe restwarmte-energie op te vangen met verbeterde polymeren
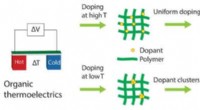
- Onderzoekers bereiken ongekende controle over polymeerroosters

- Ingenieurs vinden een nette manier om afvalkooldioxide om te zetten in bruikbaar materiaal
- Harde magneten met één molecuul:tetranucleaire zeldzame aardmetaalcomplexen met gigantische spin

 Waarom zwelt en barst beton?
Waarom zwelt en barst beton? Luchtmacht certificeert eerste 3D-geprinte niet-structurele vliegtuigonderdelen
Luchtmacht certificeert eerste 3D-geprinte niet-structurele vliegtuigonderdelen Een keerpunt in lithium-zwavel batterijveldtechnologie
Een keerpunt in lithium-zwavel batterijveldtechnologie Welke massa zuurstof bevat hetzelfde aantal moleculen als 42 g stikstof?
Welke massa zuurstof bevat hetzelfde aantal moleculen als 42 g stikstof?  Zullen brede binaire bestanden het einde van MOND betekenen?
Zullen brede binaire bestanden het einde van MOND betekenen?  Kan Iowa ooit de maan- en zonne -zonsverduistering zien?
Kan Iowa ooit de maan- en zonne -zonsverduistering zien?  Hoe lichaamsboerderijen werken
Hoe lichaamsboerderijen werken  Wat beschrijft de capaciteit het beste?
Wat beschrijft de capaciteit het beste?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

