
Wetenschap
Hoeveel elektronen zullen fluor delen om covalente bindingen te laten voltooien zijn buitenste energieniveau?
Fluorine zal één delen Elektron om zijn buitenste energieniveau te voltooien.
Dit is waarom:
* Fluor's Electron Configuration: Fluor heeft 9 elektronen, met de configuratie 2, 7. Dit betekent dat het 7 elektronen heeft in de buitenste schaal (valentieschaal).
* octetregel: Atomen hebben de neiging om elektronen te winnen, te verliezen of te delen om een stabiele configuratie van 8 elektronen in hun valentieschil (octetregel) te bereiken.
* delen voor stabiliteit: Fluor heeft nog een elektron nodig om een volledig octet te bereiken. Het bereikt dit door het ene elektron te delen met een ander atoom en een enkele covalente binding te vormen.
Laat het me weten als je andere voorbeelden van covalente binding wilt verkennen!
 Onderzoekers tonen de impact van COVID-19 en klimaatverandering op de drinkwaterkwaliteit in Berlijn
Onderzoekers tonen de impact van COVID-19 en klimaatverandering op de drinkwaterkwaliteit in Berlijn  Elektrochemische cel haalt lithium uit zeewater
Elektrochemische cel haalt lithium uit zeewater Gebruikmaken van de structuur van bacteriële gastheercelreceptoren om kanker te detecteren
Gebruikmaken van de structuur van bacteriële gastheercelreceptoren om kanker te detecteren Nieuwe authenticatiemethode voor de identificatie van β-sitosterol in eetbare oliën
Nieuwe authenticatiemethode voor de identificatie van β-sitosterol in eetbare oliën  Waar worden de metalliods gevonden op het periodieke tabel?
Waar worden de metalliods gevonden op het periodieke tabel?
 NASA ziet de zwaarste regenval in tropische cycloon Calebs
NASA ziet de zwaarste regenval in tropische cycloon Calebs Wereld verlengt reeks warmterecords voor de elfde maand op rij
Wereld verlengt reeks warmterecords voor de elfde maand op rij  Zinkende Amerikaanse steden die meer worden blootgesteld aan de stijgende zeespiegel:studie
Zinkende Amerikaanse steden die meer worden blootgesteld aan de stijgende zeespiegel:studie  Lessen uit het Aliso Canyon-lek
Lessen uit het Aliso Canyon-lek Demystificatie van de complexe aard van arctische wolken
Demystificatie van de complexe aard van arctische wolken
Hoofdlijnen
- Welk bestanddeel hebben alle basen gemeen?
- Wat zijn de chemische zintuigen?
- Hoe communiceren vogels? Netwerkwetenschappelijke modellen openen nieuwe mogelijkheden voor experts
- Psychologische theorie over de vijf menselijke zintuigen
- De structuur en functie van mRNA
- Het chocoladeaanbod ter wereld wordt bedreigd door een verwoestend virus
- Wat gebeurt er met het resulterende polypeptide wanneer 1 nucleotidepaar verloren gaat vanuit het midden van coderende sequentie een gen?
- Nachtvliegers of dagjesmensen? Studie werpt licht op wanneer motten, vlinders zijn actief
- Welke term verwijst naar organismen die worden gebruikt om de gezondheid van het milieu te bewaken?
- Heterogene katalysator wordt enzymatisch
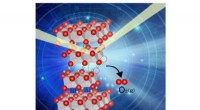
- Het voorkomen van zuurstofafgifte leidt tot veiligere batterijen met een hoge energiedichtheid
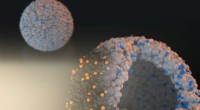
- Een moleculaire routekaart naar het immuunsysteem van planten

- Beoordeling van het begin van calciumfosfaatkiemvorming door gehyperpolariseerde real-time NMR

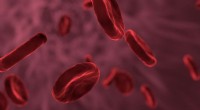
- Nieuwe test vindt nieuw mechanisme dat ten grondslag ligt aan veroudering van rode bloedcellen
 LA's grootste aardbevingsdreiging bevindt zich op een over het hoofd gezien deel van San Andreas, studie zegt. Dat kan goed zijn
LA's grootste aardbevingsdreiging bevindt zich op een over het hoofd gezien deel van San Andreas, studie zegt. Dat kan goed zijn Afbeelding:röntgenbronnen in de tweede zwenkcatalogus van XMM-Newton
Afbeelding:röntgenbronnen in de tweede zwenkcatalogus van XMM-Newton Welk proces wordt door wetenschappers gebruikt om antwoorden en vragen te vinden of een probleem op te lossen?
Welk proces wordt door wetenschappers gebruikt om antwoorden en vragen te vinden of een probleem op te lossen?  Hackers maken gepersonaliseerde ransomware om de meest winstgevende en kwetsbaren te targeten
Hackers maken gepersonaliseerde ransomware om de meest winstgevende en kwetsbaren te targeten De eetlust voor snelle mode raakt uit de mode wanneer mensen leren over de impact van in massa geproduceerde kleding, studie toont
De eetlust voor snelle mode raakt uit de mode wanneer mensen leren over de impact van in massa geproduceerde kleding, studie toont Onderzoek maakt topologische isolatoren magnetisch ruim boven kamertemperatuur
Onderzoek maakt topologische isolatoren magnetisch ruim boven kamertemperatuur Het pad naar de zuurgraad van wijnen ontdekken
Het pad naar de zuurgraad van wijnen ontdekken Nieuwe elektrodepositiemethode met atomaire laag levert verrassende resultaten op
Nieuwe elektrodepositiemethode met atomaire laag levert verrassende resultaten op
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

