
Wetenschap
Kun je waterstof en zuurstof creëren zonder water te gebruiken?
1. Elektrolyse van andere verbindingen:
* elektrolyse van gesmolten metaaloxiden: Bepaalde metaaloxiden, zoals lithiumoxide (li₂o), kunnen in hun gesmolten toestand worden geëlektolyseerd. Dit proces breekt het oxide af in zijn samenstellende elementen en produceert zuurstofgas aan de anode en lithiummetaal bij de kathode.
* elektrolyse van zuren: Sommige zuren, zoals zwavelzuur (h₂so₄), kunnen worden geëlektolyseerd om waterstofgas te produceren bij de kathode en zuurstofgas aan de anode. Dit proces is echter minder efficiënt dan elektrolyse van water en kan gevaarlijker zijn.
2. Chemische reacties:
* Thermische ontleding van metaaloxiden: Bepaalde metaaloxiden, zoals kwikoxide (HGO), ontleden in hun elementen wanneer ze worden verwarmd. Verwarming HGO brengt kwik en zuurstofgas vrij.
* Ontleding van waterstofperoxide: Waterstofperoxide (H₂o₂) kan uiteenvallen in water en zuurstofgas in aanwezigheid van een katalysator zoals mangaandioxide. Dit proces wordt gebruikt in sommige raketbrandstoffen.
3. Fotolyse:
* Fotolyse van water: Deze methode gebruikt lichte energie om watermoleculen direct in waterstof en zuurstof te breken. Het is een veelbelovend gebied van onderzoek voor productie van duurzame energie.
Opmerking: Hoewel deze methoden waterstof en zuurstof kunnen genereren, zijn ze vaak complexer, kostbaarder en minder efficiënter dan het gebruik van waterelektrolyse. Water is de meest voorkomende bron van waterstof en zuurstof, waardoor het de meest praktische optie is voor de meeste toepassingen.
 Hoeveel H-atomen zijn aanwezig in 5 moleculen propaan?
Hoeveel H-atomen zijn aanwezig in 5 moleculen propaan?  Waarom maken regeringen wetten over het gebruik van chemicaliën waarvan bekend is dat ze als mutagenen zijn?
Waarom maken regeringen wetten over het gebruik van chemicaliën waarvan bekend is dat ze als mutagenen zijn?  Poreus kristal leidt reactie om koolstofdioxide te transformeren
Poreus kristal leidt reactie om koolstofdioxide te transformeren Wat is een overgangselement uit periode 4 dat 3 diamagnetische ionen vormt?
Wat is een overgangselement uit periode 4 dat 3 diamagnetische ionen vormt?  Wat zijn de producten van zuur gekatalyseerde hydolyse een vet?
Wat zijn de producten van zuur gekatalyseerde hydolyse een vet?
 Recente studies vinden voorheen onbekend verlies van Antarctisch ijs
Recente studies vinden voorheen onbekend verlies van Antarctisch ijs Onderzoek naar verbanden tussen drie aardbevingen in Nieuw-Zeeland
Onderzoek naar verbanden tussen drie aardbevingen in Nieuw-Zeeland Potentieel voor natuurlijke hergroei van bossen om koolstof vast te leggen
Potentieel voor natuurlijke hergroei van bossen om koolstof vast te leggen Hoe het Chicxulub-impactor aanleiding gaf tot moderne regenwouden
Hoe het Chicxulub-impactor aanleiding gaf tot moderne regenwouden De droogtesituatie in Kaapstad begrijpen
De droogtesituatie in Kaapstad begrijpen
Hoofdlijnen
- Wat ondergaat gentherapie?
- Wat doet te veel homogenisatie van bacteriën?
- Ideeën voor het maken van een 3D-model van een cel
- Welke organel bevat spijsverteringsenzymen en helpen om afval in de cel te verteren?
- Hebben beide organismen voordelen in een relatie met mutualisme?
- Welk ene kenmerk scheidt koninkrijken archebacteriën en eubacteriën van het hele andere koninkrijk?
- Welke elementen worden gevonden in de biosfeer?
- Dierenartsen voeren de eerste bekende hersenoperatie uit om hydrocephalus bij pelsrobben te behandelen
- Onderzoekers ontdekken hoe cellen decennia later infecties onthouden
- Nieuwe coating brengt lithium-metaalbatterij dichter bij de realiteit

- Zou de hitte van de aardkorst de ultieme energiebron kunnen worden?

- Onderzoekers boeken belangrijke vooruitgang bij het printen van circuits op draagbare stoffen

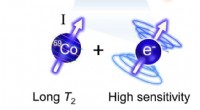
- Chemici ontwerpen chemische sonde voor het detecteren van minieme temperatuurverschuivingen in het lichaam
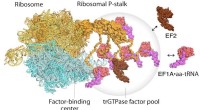
- High-speed atomic force microscopie visualiseert celeiwitfabrieken
 Metaallitteken gevonden op kannibaalster
Metaallitteken gevonden op kannibaalster  Diamanten zijn niet alleen meer voor sieraden
Diamanten zijn niet alleen meer voor sieraden Wat is ijzercarbonaat?
Wat is ijzercarbonaat?  De dikte van een rechthoekige plaat berekenen
De dikte van een rechthoekige plaat berekenen  Nieuw onderzoek identificeert de belangrijkste wereldwijde supply chain-koppelingen
Nieuw onderzoek identificeert de belangrijkste wereldwijde supply chain-koppelingen Hoe maak je een Giraf Diorama
Hoe maak je een Giraf Diorama Werknemers in de VS missen vaak ziekteverlof en gezondheidszorg - voordelen die in de meeste andere landen als vanzelfsprekend worden beschouwd
Werknemers in de VS missen vaak ziekteverlof en gezondheidszorg - voordelen die in de meeste andere landen als vanzelfsprekend worden beschouwd Waarom verliezen we Louisiana?
Waarom verliezen we Louisiana?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

