
Wetenschap
WH zijn koolstof en silicium terughoudend om ionische bindingen te vormen?
1. Hoge ionisatie -energieën:
- Koolstof en silicium hebben relatief hoge ionisatie -energieën, wat betekent dat het een aanzienlijke hoeveelheid energie vereist om een elektron uit hun atomen te verwijderen.
- Dit maakt het energetisch ongunstig voor hen om elektronen te verliezen en positieve ionen te vormen.
2. Lage elektronenaffiniteiten:
- Zowel koolstof als silicium hebben lage elektronenaffiniteiten, wat betekent dat ze niet gemakkelijk elektronen krijgen.
- Dit maakt het moeilijk voor hen om negatieve ionen te vormen.
3. Covalente bindingsvoorkeur:
- Vanwege hun positie in het periodieke tabel hebben koolstof en silicium een sterke neiging om covalente bindingen te vormen.
- Covalente binding omvat het delen van elektronen tussen atomen, wat energetisch gunstig is voor deze elementen.
4. Grote atoomstralen:
- Koolstof en silicium hebben relatief grote atoomstralen, wat leidt tot een zwakkere elektrostatische aantrekkingskracht tussen de kern- en valentie -elektronen.
- Dit maakt het moeilijker voor hen om stabiele ionische verbindingen te vormen.
5. Elektronegativiteit:
- Hoewel koolstof en silicium een matige elektronegativiteit hebben, zijn ze niet zo elektronegatief als elementen zoals zuurstof of fluor, die gemakkelijk ionische bindingen vormen.
Samenvattend: De combinatie van hoge ionisatie -energieën, lage elektronenaffiniteiten, een voorkeur voor covalente binding, grote atoomstralen en matige elektronegativiteit maakt het energetisch ongunstig voor koolstof en silicium om ionische bindingen te vormen. Ze nemen gemakkelijk deel aan covalente binding en vormen een breed scala aan organische en anorganische verbindingen.
 Hoe Romeinse cijfers in de chemie te gebruiken Nomenclatuur
Hoe Romeinse cijfers in de chemie te gebruiken Nomenclatuur Wetenschappers kijken toe hoe kunstmatige atomen samenkomen in perfecte roosters met vele toepassingen
Wetenschappers kijken toe hoe kunstmatige atomen samenkomen in perfecte roosters met vele toepassingen Welke dingen kunnen mensen gebruiken om theorieën te bespreken over hoe en waarom atomen banden vormen?
Welke dingen kunnen mensen gebruiken om theorieën te bespreken over hoe en waarom atomen banden vormen?  Hoe een gigantische 'thermosfles' zal helpen bij het begrijpen van antimaterie
Hoe een gigantische 'thermosfles' zal helpen bij het begrijpen van antimaterie  Hydrogel 3D-print- en patroonvloeistoffen met het condensatorrandeffect (PLEEC)
Hydrogel 3D-print- en patroonvloeistoffen met het condensatorrandeffect (PLEEC)
 De ondergrondse effecten van aardbevingen en vulkanen
De ondergrondse effecten van aardbevingen en vulkanen Grommen of fluiten:Succesvolle honingjagers weten hoe ze moeten communiceren met wilde honingzoekende vogels
Grommen of fluiten:Succesvolle honingjagers weten hoe ze moeten communiceren met wilde honingzoekende vogels  Hout en bladeren rot om humus fysisch of chemisch te vormen?
Hout en bladeren rot om humus fysisch of chemisch te vormen?  NASA onderzoekt de regenval van de tropische storm Kong-Reys
NASA onderzoekt de regenval van de tropische storm Kong-Reys Voor- en nadelen van natuurlijke omgevingen
Voor- en nadelen van natuurlijke omgevingen
Hoofdlijnen
- Mutaties zoals polyploïdie en cross-over vormen de genetische basis voor?
- Wanneer afscheid nemen? Enquête werpt licht op moeilijke beslissingen voor hondenbezitters
- Hoe zijn cellen, weefsels en organen aan elkaar gerelateerd?
- Wat betekent classiflying in de wetenschap?
- Het ontdekken van één reden waarom zwermen evolueerden, biedt verleidelijke aanwijzingen over hoe intelligentie zich ontwikkelde
- Wat is een ongeldige hypothese?
- Wat zijn de zes menselijke zintuigen?
- Hoe cellen delen en zich voortplanten?
- Wetenschappers manipuleren de Set2-route om te laten zien hoe genen getrouw worden gekopieerd
- Van maïs tot vlok:gezondheidsbevorderende fenolzuren die verloren gaan tijdens voedselverwerking

- Nieuwe lipidevormatlas is de sleutel tot vroege ziektedetectie

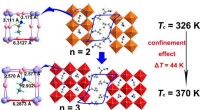
- Onderzoekers verwerven gelaagde metaalhalogenide-ferro-elektriciteit met hoge Curie-temperatuur via kooi-begrensde ethylaminerotators
- Magnetische tanden zijn veelbelovend voor materialen en energie

- Dragende verstrikkingen in polymeerglazen

 Is chloroform mengbaar met petroleumether?
Is chloroform mengbaar met petroleumether?  Wat is de Griekse oorsprong van de levenstheorie?
Wat is de Griekse oorsprong van de levenstheorie?  Welvaart doodt de planeet, waarschuw wetenschappers
Welvaart doodt de planeet, waarschuw wetenschappers Eenvoudige interventies kunnen mensen helpen valse krantenkoppen te herkennen
Eenvoudige interventies kunnen mensen helpen valse krantenkoppen te herkennen Een fris wiskundig perspectief opent nieuwe mogelijkheden voor computationele chemie
Een fris wiskundig perspectief opent nieuwe mogelijkheden voor computationele chemie Orkaan Maria gaf ecologen een zeldzame kans om te bestuderen hoe tropische droge bossen zich herstellen
Orkaan Maria gaf ecologen een zeldzame kans om te bestuderen hoe tropische droge bossen zich herstellen  Guam vermijdt ernstige koraalverbleking voorspeld voor dit jaar
Guam vermijdt ernstige koraalverbleking voorspeld voor dit jaar Wat is een stationaire geluidsbron?
Wat is een stationaire geluidsbron?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

