
Wetenschap
Waarom is de pH-schaal 1-14 en niet 1-10 of iets intuïtiever?
* Logaritmische schaal: De pH -schaal is een logaritmische schaal, wat betekent dat elke gehele getalverandering een tienvoudige verandering vertegenwoordigt in de concentratie van H+ -ionen. Dit stelt ons in staat om een breed scala aan zuurgraad en alkaliteit op een beheersbare manier uit te drukken.
* Autoionisatie van het water: Water zelf kan een beetje ioniseren en H+ en OH-ionen produceren. Het product van hun concentraties is een constante (KW) bij een gegeven temperatuur. Bij 25 ° C, KW =1 x 10^-14.
* Neutrale pH: De neutrale pH van 7 komt overeen met gelijke concentraties van H+ en OH-ionen in water. Dit komt omdat de vierkantswortel van 1 x 10^-14 1 x 10^-7 is, die de concentratie van elk ion vertegenwoordigt.
* uitersten:
* pH 1: Vertegenwoordigt een zeer zure oplossing met een H+ -concentratie van 1 x 10^-1 M.
* pH 14: Vertegenwoordigt een zeer eenvoudige oplossing met een H+ -concentratie van 1 x 10^-14 M.
Waarom niet 1-10?
Het gebruik van een schaal van 1-10 zou het bereik van zuurgraad en alkaliteit comprimeren. Het verschil tussen een pH van 1 en 2 zou veel groter zijn dan het verschil tussen een pH van 9 en 10. Dit zou niet nauwkeurig de werkelijke veranderingen in H+ -concentratie weerspiegelen.
Samenvattend:
De pH-schaal is 1-14 omdat het een logaritmische schaal is op basis van de concentratie van H+ -ionen in water. Dit bereik stelt ons in staat om een breed scala van zuurgraad en alkaliteit uit te drukken met behoud van een consistent verband tussen pH -waarden en H+ -concentraties.
Hoofdlijnen
- Wat is een andere naam voor een trofisch niveau?
- Zijn eicellencellen haploïd of diploïd?
- Een bepaalde genenpool bevat slechts twee allelen G en H voor een erfelijke eigenschap als allel een relatieve frequentie van 42 procent heeft Wat is de H?
- Is een chloropast plantencel of dier beide?
- Het transcriptoom van een schadelijk onkruid samenstellen:nieuwe bronnen om te bestuderen hoe planten binnendringen
- Wat gebeurt er met eiwitten nadat ze in de ruwe ER zijn gesynthetiseerd?
- Officiële vishandel onderschat wereldwijde vangsten enorm
- Waarom de tropische zeeën van Azië en de Stille Oceaan vol zitten met zeeleven
- Noem de structuur aan de rand van cytoplasma epitheelcellen genomen uit je binnenwang?
- Zijden micrococons kunnen worden gebruikt in de biotechnologie en geneeskunde

- Turing-structuren in een door mensen gemaakte interface

- Zodra we de CO2-uitstoot kunnen opvangen, dit is wat we ermee kunnen doen
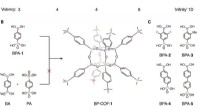
- Nieuw covalent organisch raamwerk met boor en fosfor zorgt voor betere connectiviteit
- Met behulp van computationele chemie om goedkopere infrarood plastic lenzen te produceren

 Wat voor soort landvormen creëren secundaire krachten?
Wat voor soort landvormen creëren secundaire krachten?  Twee koala's gered in bosbrand in Australië, lot 100s onbekend
Twee koala's gered in bosbrand in Australië, lot 100s onbekend Akkoord! Verre branden laten de hoofdstad van Californië in een waas achter
Akkoord! Verre branden laten de hoofdstad van Californië in een waas achter Een magneto-optische modulator zou de ontwikkeling van op supergeleiders gebaseerde computers van de volgende generatie kunnen vergemakkelijken
Een magneto-optische modulator zou de ontwikkeling van op supergeleiders gebaseerde computers van de volgende generatie kunnen vergemakkelijken Nieuwe techniek biedt moleculaire beeldvorming en analyse met hogere resolutie
Nieuwe techniek biedt moleculaire beeldvorming en analyse met hogere resolutie Kunnen verschillende allelen een enkele eigenschap beïnvloeden?
Kunnen verschillende allelen een enkele eigenschap beïnvloeden?  Verschil tussen een coëfficiënt en een subscript
Verschil tussen een coëfficiënt en een subscript Zwaartekrachtgolven opnieuw gevonden:zo konden ze de geheimen van het universum fluisteren
Zwaartekrachtgolven opnieuw gevonden:zo konden ze de geheimen van het universum fluisteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


