
Wetenschap
Wat beschrijft een chemische reactie correct die het evenwicht heeft bereikt?
Key -kenmerken van evenwicht
* Voorwaartse en omgekeerde tarieven zijn gelijk: De snelheid waarmee reactanten worden in producten (voorwaartse reactie) is exact hetzelfde als de snelheid waarmee producten weer in reactanten veranderen (omgekeerde reactie). Dit betekent dat er geen netto verandering is in de hoeveelheden reactanten en producten.
* constante concentraties: Terwijl de reacties doorgaan, blijven de concentraties van reactanten en producten in de loop van de tijd constant.
* Dynamisch proces: Evenwicht is geen statische toestand waar reacties stoppen. Het is een dynamische balans waarbij de voorwaartse en omgekeerde reacties met dezelfde snelheid plaatsvinden, wat resulteert in geen waarneembare verandering.
* Omkeerbare reacties: Evenwicht is alleen mogelijk voor reacties die omkeerbaar zijn. Dit betekent dat de producten opnieuw kunnen reageren om reactanten te vormen.
* evenwichtsconstante (KC): Een specifieke verhouding van productconcentraties tot reactantconcentraties bij evenwicht, die constant is voor een gegeven temperatuur.
Voorbeeld
Stel je een reactie voor waarbij A + B <=> C + D
Bij evenwicht:
* De snelheid van A + B die in C + D verandert, is hetzelfde als de snelheid van C + D verandert in A + B.
* De concentraties van A, B, C en D blijven constant.
Belangrijke opmerking: Hoewel de concentraties constant zijn in evenwicht, hoeven ze niet noodzakelijkerwijs gelijk te zijn. De relatieve hoeveelheden reactanten en producten in evenwicht zijn afhankelijk van de evenwichtsconstante voor de reactie.
 Leuke wetenschapsprojecten voor 7- tot 8-jarigen
Leuke wetenschapsprojecten voor 7- tot 8-jarigen Plastic dat de planeet redt? Nieuwe hars voor startups helpt de industrie groen te worden
Plastic dat de planeet redt? Nieuwe hars voor startups helpt de industrie groen te worden Nieuwe experimentele strategie verheldert complexe kristalstructuur
Nieuwe experimentele strategie verheldert complexe kristalstructuur Wat is het chemische dikoolstofhexahydride?
Wat is het chemische dikoolstofhexahydride?  Heet spul:een nieuw thermisch pad voor een hoog explosief
Heet spul:een nieuw thermisch pad voor een hoog explosief
 Plantaardige vliegtuigbrandstof kan de uitstoot met 68% verminderen
Plantaardige vliegtuigbrandstof kan de uitstoot met 68% verminderen Grote Meren blijven stijgen; meren Michigan, Huron zal waarschijnlijk de records van september overtreffen
Grote Meren blijven stijgen; meren Michigan, Huron zal waarschijnlijk de records van september overtreffen Wat is het meest erkende element van kunst?
Wat is het meest erkende element van kunst?  Wat eet de harp zeehonden?
Wat eet de harp zeehonden?  VS, Mexico beloven een half miljard dollar om grensoverschrijdende vervuiling door afvalwater van de Tijuana-rivier te bestrijden
VS, Mexico beloven een half miljard dollar om grensoverschrijdende vervuiling door afvalwater van de Tijuana-rivier te bestrijden
Hoofdlijnen
- Nucleaire divisie waarin het chromosoom wordt gereduceerd van 2n tot n onderdeel van de levenscyclus alle organismen behalve vormen varens insecten bacteriën of protozoën?
- Rijden over vlees, troost vinden bij vrienden:de emoties van de mensapen
- Wat is de basiseenheid van structuur in protisten en monerans?
- Wat is het verschil tussen de biologische term fitness en de algemene betekenis van het woord?
- Uit onderzoek blijkt hoe vrouwtjes het 'juiste' sperma kiezen
- Wat maakt de structuur van spiercellen anders dan andere cellen?
- Organisme dat de voedingsstoffen van dode organismen afbreekt of voedsel verspilt?
- Wat is een proces dat soorten categoriseert door hun genetische materiaal te onderzoeken?
- Waarom veel cellen beter zijn dan één
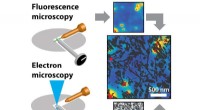
- Onderzoeker volgt nauwkeurig bewegingen van een enkel katalysatordeeltje
- Er komt iets slecht (ruikend) op deze manier - de wetenschap van stoffen en geuren

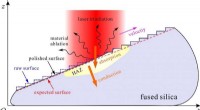
- CO2-laserablatie leidt een nieuw pad naar aangepaste continue gesmolten silica-oppervlakken
- structurele kleuren, zonder de glans

- Zelfaangedreven op papier gebaseerde SPED's kunnen leiden tot nieuwe medisch-diagnostische hulpmiddelen

 Koolhydraten omzetten in lipiden voor biobrandstoffen voor microalgen
Koolhydraten omzetten in lipiden voor biobrandstoffen voor microalgen Is de wetenschap slaap aan het uitfaseren?
Is de wetenschap slaap aan het uitfaseren?  Hoe ongelijkheden met intervalnotatie op te lossen
Hoe ongelijkheden met intervalnotatie op te lossen Vluchten weer opgeschort op London Gatwick na dronemelding
Vluchten weer opgeschort op London Gatwick na dronemelding Een nieuwe techniek die kwantumlicht gebruikt om temperatuur op nanoschaal te meten
Een nieuwe techniek die kwantumlicht gebruikt om temperatuur op nanoschaal te meten Welk type sculptuur is locatiespecifiek en ontworpen om de perceptie een ruimte te transformeren?
Welk type sculptuur is locatiespecifiek en ontworpen om de perceptie een ruimte te transformeren?  Engineering van 2D-halfgeleiders met ingebouwde geheugenfuncties
Engineering van 2D-halfgeleiders met ingebouwde geheugenfuncties Onderzoeker creëert een ultraeenvoudige goedkope methode om optische vezels te fabriceren
Onderzoeker creëert een ultraeenvoudige goedkope methode om optische vezels te fabriceren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

