
Wetenschap
Waarom is ammoniumchloride oplosbaar in water?
1. ION-DIPOLE-interacties:
* Ammoniumchloride is een ionische verbinding, wat betekent dat het bestaat als ionen (NH₄⁺ en CL⁻) in zijn vaste vorm.
* Water is een polair molecuul met een gedeeltelijke positieve lading op de waterstofatomen en een gedeeltelijke negatieve lading op het zuurstofatoom.
* De positief geladen ammoniumionen (NH₄⁺) worden aangetrokken tot het negatief geladen zuurstofatoom van watermoleculen.
* Evenzo worden de negatief geladen chloride -ionen (CL⁻) aangetrokken tot de positief geladen waterstofatomen van watermoleculen.
* Deze sterke ion-dipool interacties overwinnen de ionische krachten die het ammoniumchloride-kristal tegen elkaar houden, waardoor het kan oplossen.
2. Hydratatie:
* Wanneer ammoniumchloride oplost in water, omringen watermoleculen de ionen en vormen ze een hydratatieschaal.
* Dit hydratatieproces verzwakt de ionische bindingen in het ammoniumchloridekristal en helpt de ionen in oplossing gescheiden te houden.
3. Entropie:
* De oplossing van ammoniumchloride in water verhoogt de entropie (aandoening) van het systeem.
* Deze toename van entropie is gunstig en draagt bij aan de oplosbaarheid van het zout.
Over het algemeen:
De combinatie van sterke ion-dipoolinteracties, hydratatie van ionen en de entropie-toename geassocieerd met het oplossen van ammoniumchloride in water leidt tot zijn hoge oplosbaarheid.
 Ammoniak:een troef voor het energietransitieproces
Ammoniak:een troef voor het energietransitieproces Moleculaire interacties meten
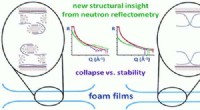
Moleculaire interacties meten Een schijnwerper schijnen op de machinerie van het leven
Een schijnwerper schijnen op de machinerie van het leven Hoeveel mol koolstof zit er in 35 g aluminiumacetaat?
Hoeveel mol koolstof zit er in 35 g aluminiumacetaat?  Onderzoekers beoordelen geminiaturiseerde elektrochemische sensortechnologieën voor snelle detectie van zware metalen
Onderzoekers beoordelen geminiaturiseerde elektrochemische sensortechnologieën voor snelle detectie van zware metalen
Hoofdlijnen
- Staafvormige structuur gemaakt van DNA?
- Wat is een schulling?
- Wat betekent verkiezing in de wetenschap?
- Wat is de wetenschap achter Apple Project?
- Snelle reactie van Fish op klimaatverandering
- Waarom maken we verkeerde keuzes?
- Onderzoekers brengen de dynamiek van eiwitnetwerken tijdens celdeling in kaart
- Biomassa versus energiepiramides
- Wat bevordert de opslag van glucose als glycogeen?
- Proost! Wetenschappers zetten grote stap in de richting van het perfecte bierhoofd
- Betaalbare en mobiele zuivering van dialysewater
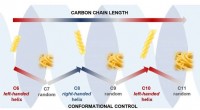
- Koolstofketens nemen fusilli- of spaghetti-vormen aan als ze oneven of even getallen hebben
- Vormveranderend element vormt de sleutel tot antibacteriële coating

- Gelijktijdige meting van biofysische eigenschappen en positie van afzonderlijke cellen in een microdevice

 De legalisatie van marihuana in Oregon leidde tot een grote daling van de verkoop in de grensregio's van Washington
De legalisatie van marihuana in Oregon leidde tot een grote daling van de verkoop in de grensregio's van Washington Wetenschappers bieden nieuwe theorieën over hoe planten de ritmes van licht kunnen orkestreren
Wetenschappers bieden nieuwe theorieën over hoe planten de ritmes van licht kunnen orkestreren  Zoeken naar leven op Mars kan een door water versterkte boost krijgen
Zoeken naar leven op Mars kan een door water versterkte boost krijgen Onderzoekers nemen opto-elektronische diodes op in vezels en weven ze in wasbare stoffen
Onderzoekers nemen opto-elektronische diodes op in vezels en weven ze in wasbare stoffen Verblindende aurorae verdwijnen uit de hemel terwijl de zonnevlek zich afwendt
Verblindende aurorae verdwijnen uit de hemel terwijl de zonnevlek zich afwendt  Het in kaart brengen van de beste route voor een ruimtevaartuig dat buiten de invloedssfeer van de zon reist
Het in kaart brengen van de beste route voor een ruimtevaartuig dat buiten de invloedssfeer van de zon reist  Experimenteel behandelregime effectief tegen hiv
Experimenteel behandelregime effectief tegen hiv Is drijfzand echt? Ontdek hoe drijfzand werkt
Is drijfzand echt? Ontdek hoe drijfzand werkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

