
Wetenschap
Studie onthult mogelijk nieuw behandeldoel in de strijd tegen COVID-19
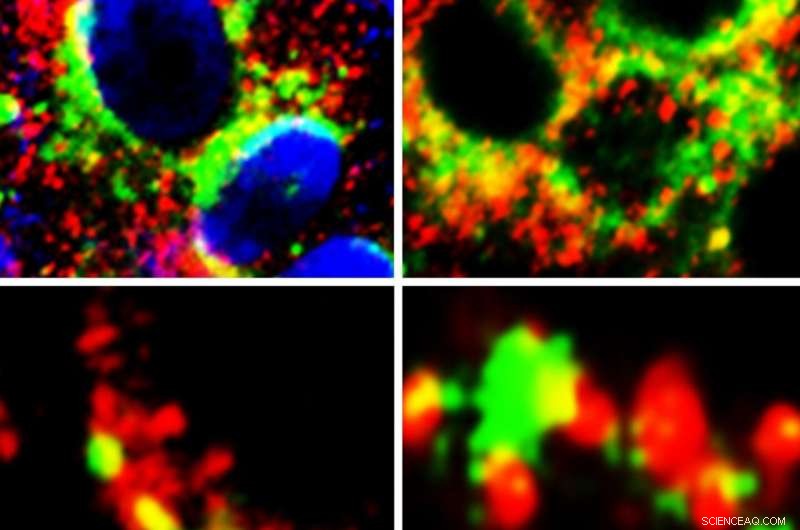
Cellen die de nabijheid (geel) van GRP78 (groen) met Spike-eiwit van SARS-Cov-2 (rood) (linkerpanelen) en ACE2 (rood) (rechterpanelen) vertonen. Credit:hoofdauteur Anthony Carlos, PhD
De snelle ontwikkeling van vaccins heeft een essentieel instrument opgeleverd om de verspreiding van het dodelijke SARS-CoV-2-virus tegen te gaan, maar uitdagingen om groepsimmuniteit te bereiken, veroorzaakt door de opkomst van nieuwe mutaties en het onvermogen van mensen met een onderdrukt immuunsysteem om een effectieve immuunrespons te ontwikkelen na vaccinatie, wijzen op een behoefte aan aanvullende oplossingen om de bescherming te maximaliseren.
Een nieuwe USC-studie gepubliceerd in de Tijdschrift voor biologische chemie onthult hoe therapieën die gericht zijn op een moleculaire chaperonne, GRP78 genaamd, extra bescherming kunnen bieden tegen COVID-19 en andere coronavirussen die in de toekomst opduiken.
Chaperones zoals GRP78 zijn moleculen die helpen bij het reguleren van de juiste vouwing van eiwitten, vooral wanneer een cel onder stress staat. Maar in sommige gevallen, virussen kunnen deze chaperonnes kapen om doelcellen te infecteren, waar ze zich voortplanten en verspreiden. GRP78 is betrokken bij de verspreiding van andere ernstige virussen, zoals ebola en zika.
GRP78 speelt meer dan één rol bij COVID-19
Hoewel studies hebben aangetoond dat SARS-CoV-2, het virus dat COVID-19 veroorzaakt, infecteert cellen door te binden met ACE2-receptoren op hun oppervlak, onderzoekers van de Keck School of Medicine van USC onderzochten of GRP78 ook een rol speelt.
Ze ontdekten dat GRP78 dient als een co-receptor en stabilisator tussen ACE2 en SARS-CoV-2, het verbeteren van de herkenning van het spike-eiwit van het virus en het mogelijk maken van efficiëntere virale toegang tot gastheercellen.
Deze studie levert het eerste experimentele bewijs ter ondersteuning van voorspellingen van computermodellering, wat aantoont dat GRP78 het Spike-eiwit van SARS-CoV-2 in cellen bindt. interessant, computermodellering laat verder zien dat COVID-19-varianten die besmettelijker zijn, sterker binden aan GRP78.
Aanvullend, het onderzoeksteam ontdekte dat GRP78 ook bindt aan en werkt als een regulator van ACE2, waardoor het eiwit naar het celoppervlak wordt gebracht, die SARS-CoV-2 meer punten biedt om zich aan te binden en cellen te infecteren.
"Onze studie onthult dat therapie gericht op GRP78 effectiever zou kunnen zijn in het beschermen en behandelen van mensen die COVID-19 oplopen dan alleen vaccins, vooral als het gaat om mensen die het vaccin niet kunnen krijgen en varianten die vaccinbescherming zouden kunnen omzeilen, maar toch afhankelijk zijn van GRP78 voor toelating en productie, " zei senior auteur Amy S. Lee, doctoraat, Judy en Larry Freeman Leerstoel in fundamenteel wetenschappelijk onderzoek en professor aan de afdeling biochemie en moleculaire geneeskunde aan de Keck School of Medicine van USC.
Hoe SARS-CoV-2 GRP78 kaapt
De taak van GRP78 als chaperonne-molecuul is het vouwen van eiwitten in het endoplasmatisch reticulum (ER), dat is een eiwitproductiefabriek. bij stress, inclusief stress veroorzaakt door SARS-CoV-2-infectie, GRP78 wordt naar het celoppervlak verscheept. Daar, het vergemakkelijkt de binding tussen ACE2 en Spike-eiwit van SARS-CoV-2, wat leidt tot een verhoogde virale binnenkomst. Eenmaal in de cel, Van virussen is bekend dat ze de ER-eiwitvouwmachines kapen, waarvan GRP78 een belangrijke speler is, om meer virale eiwitten te produceren.
Dit proces kan worden geïntensiveerd in cellen die onder stress staan door andere ziekten zoals diabetes of kanker, wat een van de redenen kan zijn waarom mensen met onderliggende gezondheidsproblemen vatbaarder zijn voor SARS-CoV-2-infectie.
Om de rol van GRP78 bij SARS-CoV-2-infectie te onderzoeken, onderzoekers behandelden longepitheelcellen met gehumaniseerd monoklonaal antilichaam (hMAb159), waarvan bekend is dat het GRP78 van het celoppervlak verwijdert zonder nadelige effecten in muismodellen. Interventie verwijderde GRP78 en verminderde ACE2 op het celoppervlak, het verminderen van het aantal doelen waaraan SARS-CoV-2 zich zou kunnen hechten.
Deze bevindingen leidden ertoe dat onderzoekers concludeerden dat interventies, zoals hMAb159, om het celoppervlak te verwijderen, zou GRP78 de SARS-CoV-2-infectie kunnen verminderen en de verspreiding en ernst van COVID-19 bij geïnfecteerde mensen kunnen remmen.
Potentieel voor GRP78 gerichte behandeling
Gezonde cellen hebben een fractie van GRP78 nodig om normaal te functioneren. Echter, gestresste cellen, zoals viraal geïnfecteerde of kankercellen, meer GRP78 nodig hebben om te overleven en zich te vermenigvuldigen, dus behandelingen die de hoeveelheid GRP78 in het lichaam verminderen, kunnen de ernst van SARS-CoV-2-infectie verminderen en verspreiden zonder nadelige effecten.
Hoewel deze studie een monoklonaal antilichaam gebruikte, onderzoekers zeggen dat er andere middelen zijn die kunnen worden gebruikt om de hoeveelheid of activiteit van GRP78 te verminderen, het creëren van meerdere routes voor potentiële medicijnoplossingen om GRP78 te targeten.
"Wat vooral opwindend is voor deze bevinding, is dat GRP78 een universeel doelwit zou kunnen zijn in combinatie met bestaande therapieën, niet alleen om COVID-19 te bestrijden, maar maar ook andere dodelijke virussen die voor hun besmettelijkheid afhankelijk zijn van GRP78, " zei Leen.
De volgende stap voor het onderzoeksteam is om deze bevindingen verder te onderzoeken door middel van dierstudies.
 Team krijgt inzicht in de oxidelaag van roestvrij staal
Team krijgt inzicht in de oxidelaag van roestvrij staal Onderzoekers leggen uit hoe ze biologie kunnen beheersen met licht - zonder genetica
Onderzoekers leggen uit hoe ze biologie kunnen beheersen met licht - zonder genetica Een beschermend schild voor gevoelige enzymen in biobrandstofcellen
Een beschermend schild voor gevoelige enzymen in biobrandstofcellen De locaties van protonen, neutronen en elektronen in een atomaire structuur
De locaties van protonen, neutronen en elektronen in een atomaire structuur Hoe een EDTA-oplossing te maken
Hoe een EDTA-oplossing te maken
Hoofdlijnen
- Een driedimensionaal tandmodel maken voor een schoolproject
- Aanpassen aan fluctuerende temperaturen
- Stadia van meiose met een beschrijving
- De effecten van straling op dieren
- Wat doet Choline voor het lichaam?
- Epitheliale cellen: definitie, functie, typen en voorbeelden
- Een epigenetische sleutel om gedragsverandering te ontgrendelen
- Nieuwe methode maakt bio-ethanol uit afval in bestaande installaties
- Een plantencelmodel maken met een schoenendoos
- Vloeibaar forensisch onderzoek kan leiden tot veiliger drinkwater

- Maak een sprong voorwaarts in de ontdekking en ontwikkeling van nieuwe antibiotica

- Autonome zelfgenezing gezien in piëzo-elektrische moleculaire kristallen

- Wetenschappers identificeren chemische oorzaken van vervaging van batterijcapaciteit
- Moleculaire poriën kunnen de efficiëntie van olieraffinage en farmaceutische productie verbeteren

 Verschillen en overeenkomsten tussen een seriecircuit en een parallelcircuit
Verschillen en overeenkomsten tussen een seriecircuit en een parallelcircuit Maatschappelijk verantwoord ondernemen en COVID-19:Indiase bedrijfssector onderneemt actie
Maatschappelijk verantwoord ondernemen en COVID-19:Indiase bedrijfssector onderneemt actie Hoe worden radicale uitdrukkingen en rationele exponenten gebruikt in het echte leven?
Hoe worden radicale uitdrukkingen en rationele exponenten gebruikt in het echte leven?  Eenvoudige maar effectieve manieren om klimaatverandering tegen te gaan:tips voor het dagelijks leven
Eenvoudige maar effectieve manieren om klimaatverandering tegen te gaan:tips voor het dagelijks leven Een warme relatie tussen koralen en bacteriën
Een warme relatie tussen koralen en bacteriën Een methodologie voor het mogelijk maken van forensische analyse met behulp van hypervisor-kwetsbaarhedengegevens
Een methodologie voor het mogelijk maken van forensische analyse met behulp van hypervisor-kwetsbaarhedengegevens Soorten maden
Soorten maden  Arctisch zee-ijsverlies heeft minimale invloed op extreem koud winterweer, uit onderzoek blijkt
Arctisch zee-ijsverlies heeft minimale invloed op extreem koud winterweer, uit onderzoek blijkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

