
Wetenschap
Wat zijn de producten als water wordt afgebroken door elektrolyse?
Hier is een uitsplitsing van het proces:
* elektrolyse: Dit is het proces van het gebruik van een elektrische stroom om een niet-spontane chemische reactie aan te sturen.
* Watermoleculen (H₂o): Elk watermolecuul bevat twee waterstofatomen en één zuurstofatoom.
* elektroden: Elektrolyse maakt gebruik van twee elektroden (positieve anode en negatieve kathode) ondergedompeld in het water.
* reactie: De elektrische stroom zorgt ervoor dat de watermoleculen worden gesplitst:
* Bij de kathode (negatieve elektrode) krijgen waterstofionen (H+) elektronen en vormen het waterstofgas (H₂).
* Bij de anode (positieve elektrode) verliezen zuurstofionen (o²-) elektronen en vormen zuurstofgas (O₂).
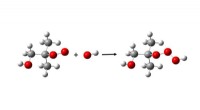
De algehele chemische vergelijking voor de elektrolyse van water is:
2h₂o → 2h₂ + o₂
Dit betekent dat voor elke twee afgebroken watermoleculen twee moleculen waterstofgas en één molecuul zuurstofgas worden geproduceerd.
 15. Waarom heeft één mol koolstofatomen een kleinere massa dan zwavelatomen?
15. Waarom heeft één mol koolstofatomen een kleinere massa dan zwavelatomen?  Wat is de druk in mm Hg van een gas bij 2 atm?
Wat is de druk in mm Hg van een gas bij 2 atm?  Coördinatiepolymeerkristallen zijn veelbelovend als nieuwe generatie lichtbronnen voor de industrie en de geneeskunde
Coördinatiepolymeerkristallen zijn veelbelovend als nieuwe generatie lichtbronnen voor de industrie en de geneeskunde  De gassen op Titan zijn allemaal ionisch gebonden. Waar of niet waar?
De gassen op Titan zijn allemaal ionisch gebonden. Waar of niet waar?  Wat was vroeger water te desinfecteren?
Wat was vroeger water te desinfecteren?
Hoofdlijnen
- Wat is het katalyserende metabole reacties in cellen?
- Waarom bestuderen mensen mariene biologie?
- Rapport benadrukt kansen en risico's in verband met synthetische biologie en bio-engineering
- Onderzoekers ontdekken dat hnRNPM de integriteit van de cellulaire eiwitproductie bewaakt
- Gebruik van microscopen in de wetenschap
- Van wat zijn chromosomen gecomponeerd?
- Menselijke evolutie: tijdlijn, stadia, theorieën en bewijsmateriaal
- Wat zijn de verschillen in sets van allelen tussen individuen die een populatie heeft genoemd?
- Wat veroorzaakte de gaten in SUE de T. rexs kaak? Waarschijnlijk geen infectie
- Bacteriën werven om katalysatoren atoom voor atoom te bouwen
- Van nata de coco tot computerschermen:Cellulose krijgt een kans om te schitteren
- Informatie extraheren uit oude tanden
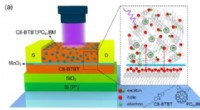
- Wetenschappers ontwikkelen ultragevoelige organische fototransistoren op basis van nieuwe hybride gelaagde architectuur
- Nieuw type extreem reactieve stof ontdekt in de atmosfeer
 Wat is de kleur van fluoriet?
Wat is de kleur van fluoriet?  Welke voordelen bieden celwanden plantencellen die contact maken met zoet water?
Welke voordelen bieden celwanden plantencellen die contact maken met zoet water?  Zwaartekrachtmissie onthult nog steeds verborgen geheimen
Zwaartekrachtmissie onthult nog steeds verborgen geheimen Studie ontrafelt het mysterie van antimicrobiële kikkersecreties
Studie ontrafelt het mysterie van antimicrobiële kikkersecreties Kosmische streepjescode van verre melkweg bevestigt de standvastigheid van de natuur
Kosmische streepjescode van verre melkweg bevestigt de standvastigheid van de natuur Heeft lachgas een dipoolmoment?
Heeft lachgas een dipoolmoment?  Wie draagt het verteerde voedsel door alle delen van het lichaam?
Wie draagt het verteerde voedsel door alle delen van het lichaam?  Wat gebeurt er als ijzersulfide reageert met verdund zwavelzuur?
Wat gebeurt er als ijzersulfide reageert met verdund zwavelzuur?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

