
Wetenschap
Wat is een super-subscript in de chemie?
Hier is een uitsplitsing:
* opladen: Superscripts worden gebruikt om de positieve of negatieve lading van een ion te tonen. In het natriumion (Na⁺) geeft het superscript " +" bijvoorbeeld een +1 -lading aan. Evenzo heeft het chloride -ion (CL⁻) een superscript " -" dat een -1 -lading aangeeft.
* Oxidatietoestand: In verbindingen worden superscripts gebruikt om de oxidatietoestand van een atoom aan te geven, dat de schijnbare lading ervan vertegenwoordigt. In het samengestelde kaliumpermanganaat (kmno₄) heeft het mangaanatoom (Mn) bijvoorbeeld een oxidatietoestand van +7, aangegeven door het superscript "VII" (Mno₄⁻¹).
belangrijke punten om te onthouden:
* Superscripts worden altijd geschreven na het chemische symbool.
* Het superscript "0" geeft een neutraal atoom of molecuul aan.
* In sommige gevallen kan het superscript een nummer zijn gevolgd door een " +" of "-" teken, bijvoorbeeld Fe²⁺, met een ijzerion met een +2 lading.
Hier zijn enkele voorbeelden:
* Na⁺ (natriumion)
* CL⁻ (chloride -ion)
* Ca²⁺ (calciumion)
* Fe³⁺ (ijzer -ion)
* Mno₄⁻¹ (permanganaat -ion)
Door superscripts in de chemie te begrijpen, kunt u de lading- en oxidatietoestanden van atomen en ionen binnen chemische verbindingen beter interpreteren.
 Ultrasnelle lasers onderzoeken ongrijpbare chemie op het vloeistof-vloeistofgrensvlak
Ultrasnelle lasers onderzoeken ongrijpbare chemie op het vloeistof-vloeistofgrensvlak Waarom verdampt water niet wanneer het in de voorverwarmde pan wordt bewaard?
Waarom verdampt water niet wanneer het in de voorverwarmde pan wordt bewaard?  Zijn boraxpoeder en caramboleboard hetzelfde?
Zijn boraxpoeder en caramboleboard hetzelfde?  Nieuwe ontdekking van cellulose kan leiden tot nieuwe chemicaliën, biobrandstoffen
Nieuwe ontdekking van cellulose kan leiden tot nieuwe chemicaliën, biobrandstoffen Kan NMR worden gedaan voor gasvormige monsters?
Kan NMR worden gedaan voor gasvormige monsters?
 Wat is het verschil tussen Caves Rock Shelter and Houses?
Wat is het verschil tussen Caves Rock Shelter and Houses?  Jonge klimaatactivisten zeggen dat hun rechtszaak voor de rechter moet komen
Jonge klimaatactivisten zeggen dat hun rechtszaak voor de rechter moet komen VN-vergadering begint met het opstellen van een plan voor een planeet zonder vervuiling
VN-vergadering begint met het opstellen van een plan voor een planeet zonder vervuiling Alle gevechten die worden gevoerd tegen infrastructuur voor fossiele brandstoffen volgen één enkele strategie
Alle gevechten die worden gevoerd tegen infrastructuur voor fossiele brandstoffen volgen één enkele strategie Wat concludeerde Darwin na zijn reis?
Wat concludeerde Darwin na zijn reis?
Hoofdlijnen
- Orginatten in het lichaam heet hoe?
- Hoeveelheid water in stamcellen kan zijn lot bepalen als vet of bot
- Welk oceaandier heeft radiale lichaamssymmetrie?
- Hoe vaak zijn er meerdere organismen geëvolueerd uit unicells?
- Is rhizoïden autotrofe voeding of hetetrofische voeding?
- Wat noemde wetenschapper de moderne kijk op celmembraanstructuur wat?
- Groter en levensechter:wat is de toekomst van biogeprinte organen?
- Gedragsstudies tonen aan dat bavianen en duiven in staat zijn tot cognitie op een hoger niveau
- Stiekeme mannetjes nemen vrouwelijke hersens aan om grote bruten voor de gek te houden
- Designer-enzym overwint sulfietreductie, een knelpunt bij het opruimen van het milieu

- Smartphone-testplekken vergiftigd waterrisico voor miljoenen levens

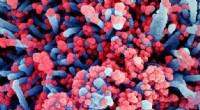
- De oppervlaktechemie van SARS-CoV-2 begrijpen
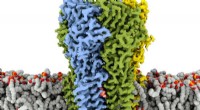
- Onderzoek geeft aan hoe algemene anesthetica en benzo's inwerken op receptoren in de hersenen
- Controleren en visualiseren van receptorsignalen in neurale cellen met licht

 Vertraging van weggelopen elektronen baant de weg voor fusie-energie
Vertraging van weggelopen elektronen baant de weg voor fusie-energie Welke twee tektonische platen vormen een convergente grens nabij Zuidoost -Azië?
Welke twee tektonische platen vormen een convergente grens nabij Zuidoost -Azië?  Astrofysici 2004-theorie bevestigd:waarom de samenstelling van de zonnen varieert
Astrofysici 2004-theorie bevestigd:waarom de samenstelling van de zonnen varieert Nieuwe nanogenerator haalt stroom uit rollende banden
Nieuwe nanogenerator haalt stroom uit rollende banden Microscopisch zicht verplaatsen naar een andere nieuwe dimensie
Microscopisch zicht verplaatsen naar een andere nieuwe dimensie Lunaire sonische knallen
Lunaire sonische knallen Nieuwe generatie supercondensatoren om groen transport te elektrificeren
Nieuwe generatie supercondensatoren om groen transport te elektrificeren Charisma uitgedaagd? Je kunt nog steeds een goede baas zijn
Charisma uitgedaagd? Je kunt nog steeds een goede baas zijn
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

