
Wetenschap
Wat zou de snelheid van reactant verminderen?
factoren die de reactiesnelheid beïnvloeden:
* het verlagen van de concentratie van reactanten: Hoe meer geconcentreerd de reactanten, hoe frequenter botsingen optreden, wat leidt tot een hogere reactiesnelheid. Het verlagen van de concentratie vermindert deze botsingen.
* het verlagen van de temperatuur: Temperatuur biedt de energie voor moleculen om activeringsenergie te overwinnen en te reageren. Het verlagen van de temperatuur vertraagt de moleculaire beweging, waardoor de frequentie en energie van botsingen worden verminderd.
* Het verhogen van de activeringsenergie: Activeringsenergie is de minimale energie die nodig is voor reactanten om producten te vormen. Het verhogen van de activeringsenergie maakt het moeilijker voor reactanten om deze barrière te overwinnen, waardoor de reactie wordt vertraagd.
* Een katalysator toevoegen (omgekeerd): Katalysatoren versnellen de reacties door een alternatieve reactieroute te bieden met een lagere activeringsenergie. Het verwijderen van een katalysator of het gebruik van een remmer heeft het tegenovergestelde effect.
* Het oppervlak van vaste stoffen verhogen: Voor reacties waarbij vaste stoffen betrokken zijn, zorgt het verhogen van het oppervlak (bijvoorbeeld door een vaste stof in kleinere deeltjes te slijpen) voor meer contactpunten voor reactanten om te interageren. Het afnemende oppervlak zal het tegenovergestelde effect hebben.
* De fase van reactanten wijzigen: Reacties in de gasfase gaan in het algemeen sneller verder dan die in de vloeibare fase, die sneller zijn dan die in de vaste fase. Het wijzigen van de fase van een meer mobiele naar een minder mobiele status zal de reactiesnelheid verlagen.
Belangrijke overwegingen:
* Reactieorder: Het specifieke effect van deze factoren op de reactiesnelheid hangt af van de volgorde van de reactie (hoe de snelheid afhangt van de concentratie van elke reactant).
* evenwicht: Hoewel deze factoren de snelheid van een reactie beïnvloeden, beïnvloeden ze ook de positie van evenwicht.
Voorbeeld:
Stel je een reactie voor waarbij twee moleculen moeten botsen om te reageren. Het verlagen van de concentratie van één reactant betekent dat er minder moleculen beschikbaar zijn om te botsen, waardoor de kansen op een succesvolle reactie worden verminderd.
Samenvattend:
Om de snelheid van een reactant te verlagen, kunt u factoren manipuleren die de frequentie en energie van botsingen tussen reactantmoleculen beïnvloeden, of de route veranderen die de reactie nodig heeft om het moeilijker te maken om de activeringsenergiebarrière te overwinnen.
 Een chemische reactie die warmte afgeeft, is het meest waarschijnlijk wat?
Een chemische reactie die warmte afgeeft, is het meest waarschijnlijk wat?  Wat is het verschil tussen vast polymeer en vloeibaar polymeer?
Wat is het verschil tussen vast polymeer en vloeibaar polymeer?  Nieuwe experimentele strategie verheldert complexe kristalstructuur
Nieuwe experimentele strategie verheldert complexe kristalstructuur "The R134a vs. the R410a
"The R134a vs. the R410a Wat is het bewijs voor een reactie wanneer natriumcarbonaat en zoutzuur zich vermengen?
Wat is het bewijs voor een reactie wanneer natriumcarbonaat en zoutzuur zich vermengen?
 Dodelijke sneeuwstormen veroorzaken chaos in heel Spanje
Dodelijke sneeuwstormen veroorzaken chaos in heel Spanje Klimaatverandering om huishoudbudgetten op te rekken
Klimaatverandering om huishoudbudgetten op te rekken De aanwezigheid van gebieden op dezelfde manier aangepaste organismen langs de kust wordt genoemd?
De aanwezigheid van gebieden op dezelfde manier aangepaste organismen langs de kust wordt genoemd?  Wetenschappers verzamelen bijna twee decennia van gletsjerijsverlies wereldwijd
Wetenschappers verzamelen bijna twee decennia van gletsjerijsverlies wereldwijd Biodiversiteit monitoren met geluid:hoe machines onze kennis kunnen verrijken
Biodiversiteit monitoren met geluid:hoe machines onze kennis kunnen verrijken
Hoofdlijnen
- Hoe worden restrictie-enzymen gebruikt?
- Onderzoek op meerdere schaal legt microben bloot die de droogtereactie van sorghum beïnvloeden
- Bindweefselcellen die fagocytisch zijn?
- Wie zijn de Forienger Scientist?
- Zou jij een mier vertrouwen om je ledemaat te amputeren? De wetenschap laat zien dat ze bekwame chirurgen zijn
- Het Hardy-Weinberg-principe stelt dat in een bevolking niet verandert tenzij externe factoren de genenpool beïnvloeden.
- Paring induceert seksuele remming bij vrouwelijke springspinnen
- Houdt mijn hond echt van mij?
- Zijn ziektekiemen en bacteriën hetzelfde?
- Verbeterde eiwitfunctie opent weg voor nieuw concept voor geneesmiddelontwikkeling
- Touchscreen-alternatief vermindert de angst voor een wereldtekort aan indium

- Exotische koolstofmicrokristallen in meteorietstof

- Wanneer mens en machine het eens zijn over iridiumoxide

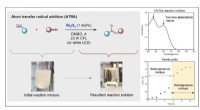
- De toekomst van op halfgeleiders gebaseerde fotokatalytische processen opfleuren
 Je hoeft geen raket te bouwen om te bewijzen dat de aarde niet plat is - hier is de simpele wetenschap
Je hoeft geen raket te bouwen om te bewijzen dat de aarde niet plat is - hier is de simpele wetenschap Lijst met ecosystemen
Lijst met ecosystemen  Welk percentage aardmassa is de innerlijke kern?
Welk percentage aardmassa is de innerlijke kern?  Wat is een prehistorische toolkit en hoe zou deze de menselijke geschiedenis kunnen herschrijven?
Wat is een prehistorische toolkit en hoe zou deze de menselijke geschiedenis kunnen herschrijven?  Landbouwgroepen dagen waarschuwing onkruidverdelger in Californië uit
Landbouwgroepen dagen waarschuwing onkruidverdelger in Californië uit Hotelgroepen begroeten nieuw offensief op Airbnb in Parijs
Hotelgroepen begroeten nieuw offensief op Airbnb in Parijs We weten nu hoe insecten en bacteriën ijs bestrijden
We weten nu hoe insecten en bacteriën ijs bestrijden Als een stuk klei van de tafel op de vloer valt, wat gebeurt er dan met de potentiële energie die het had toen het op tafel lag?
Als een stuk klei van de tafel op de vloer valt, wat gebeurt er dan met de potentiële energie die het had toen het op tafel lag?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

