
Wetenschap
Wat is een subatomair deeltje dat een chemisch gedrag of bindingsvermogen bepalen?
Dit is waarom:
* Elektronen bezetten energieniveaus en orbitalen: Elektronen zijn gerangschikt rond de kern in specifieke energieniveaus en orbitalen. Het buitenste energieniveau, de valentie -schaal genoemd, bevat valentie -elektronen.
* Valence -elektronen nemen deel aan binding: Valentie -elektronen zijn degenen die het meest waarschijnlijk interageren met andere atomen, die chemische bindingen vormen.
* Aantal valentie -elektronen bepaalt het bindgedrag: Het aantal valentie -elektronen dat een atoom heeft bepaald hoeveel bindingen het kan vormen en de soorten bindingen die het zal vormen (ionisch, covalent, enz.).
Bijvoorbeeld:
* zuurstof heeft 6 elektronen, met 2 in het eerste energieniveau en 4 in het tweede (valentie) energieniveau. Dit betekent dat het nog 2 elektronen nodig heeft om zijn valentieschaal te vullen, waardoor het zeer reactief is en waarschijnlijk twee covalente bindingen vormt.
* Natrium Heeft 1 valentie -elektron, waardoor het waarschijnlijk dat elektron verliest om een positief ion te vormen en een ionische binding te creëren.
Hoewel protonen en neutronen bijdragen aan de identiteit en stabiliteit van het atoom, zijn het de elektronen, vooral de valentie -elektronen , dat echt regeert hoe een atoom interageert met andere atomen en chemische bindingen vormt.
 Wetenschappers temmen chaotische eiwitten die 75% van de kankers voeden
Wetenschappers temmen chaotische eiwitten die 75% van de kankers voeden  Mierengedrag inspireert autonoom onderzoek naar materiaalassemblage
Mierengedrag inspireert autonoom onderzoek naar materiaalassemblage  Ontdekken hoe het toevoegen van UV-behandeling aan waterchlorering de productie van giftige trihalomethaan daadwerkelijk kan verhogen
Ontdekken hoe het toevoegen van UV-behandeling aan waterchlorering de productie van giftige trihalomethaan daadwerkelijk kan verhogen Het atoom dat overblijft nadat een neculus desinigrateert?
Het atoom dat overblijft nadat een neculus desinigrateert?  Welk polyatomisch ion wordt gebruikt, verbreken de ionische bindingen in je haar?
Welk polyatomisch ion wordt gebruikt, verbreken de ionische bindingen in je haar?
 Hoe kan een teek zich voortplanten?
Hoe kan een teek zich voortplanten?  Ontmoet Thailands geheime wapen in de strijd tegen klimaatverandering
Ontmoet Thailands geheime wapen in de strijd tegen klimaatverandering Welke invloed zullen de winden van de klimaatverandering hebben op trekvogels?
Welke invloed zullen de winden van de klimaatverandering hebben op trekvogels?  Vecht verder om de tropische wetlands van Brazilië te redden van vlammen
Vecht verder om de tropische wetlands van Brazilië te redden van vlammen Alpenbeekjes produceren meer CO2 na een warme winter
Alpenbeekjes produceren meer CO2 na een warme winter
Hoofdlijnen
- Een zich ontwikkelende plakkerige situatie
- Wat zou de chloroplast in een mobiele telefoon zijn?
- Hoe zullen chromosomen en genen het gedrag beïnvloeden?
- Protoplasma van de cellen eukaryoten is verdeeld in een afgeronde ... wat?
- Hoe visvinnen evolueerden vlak voor de overgang naar land
- Dr. YouTube... wat is uw diagnose?
- Zal het wegglijden of vastgrijpen:Wetenschappers vragen zich af:'Wat is slakkenslijm?'
- Wat is een dier dat begint met Z?
- In welke fase condenseert chromosomen en worden ze zichtbaar?
- Onderzoekers maken beter materiaal voor draagbare biosensoren

- In woestijnproeven, wateroogstmachine van de volgende generatie levert vers water uit de lucht
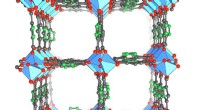
- Biogebaseerde vervangers van fossiele brandstoffen

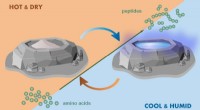
- waren heet, vochtige zomers de sleutel tot de oorsprong van het leven?
- Onderzoekers leggen in realtime rondzwervende moleculaire fragmenten vast

 Uit onderzoek blijkt dat het lidmaatschap van een partij het consumentenvertrouwen en de bestedingsintenties na verkiezingen beïnvloedt
Uit onderzoek blijkt dat het lidmaatschap van een partij het consumentenvertrouwen en de bestedingsintenties na verkiezingen beïnvloedt  Wat is er op de tap? Michigan's economie
Wat is er op de tap? Michigan's economie  Kunnen sociale netwerken consumenten helpen gezonder te worden?
Kunnen sociale netwerken consumenten helpen gezonder te worden?  Rekbaar, afbreekbare halfgeleiders
Rekbaar, afbreekbare halfgeleiders Wanneer wordt een of beide zijden van de DNA -streng gekopieerd in transcriptiei?
Wanneer wordt een of beide zijden van de DNA -streng gekopieerd in transcriptiei?  Ingenieurs overwinnen een hindernis bij het kweken van een revolutionair optisch metamateriaal
Ingenieurs overwinnen een hindernis bij het kweken van een revolutionair optisch metamateriaal B 0 C 2 D E 3 F G -Wat komt er daarna?
B 0 C 2 D E 3 F G -Wat komt er daarna?  Hoe een dwarsdoorsnede te berekenen
Hoe een dwarsdoorsnede te berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

