
Wetenschap
Hoeveel mol CO2 worden geproduceerd uit 5 mijl O2?
* mijlen zijn een afstandseenheid, niet kwantiteit. Ze meten hoe ver iets reist, niet hoeveel ervan is.
* mol zijn een eenheid van kwantiteit. Ze vertegenwoordigen een specifiek aantal moleculen (6.022 x 10^23).
Om mol CO2 te berekenen, moet u de hoeveelheid O2 weten in een meetbare eenheid zoals gram of liters.
Hier is hoe u het probleem zou benaderen als u de massa O2: had
1. Evenwichtige chemische vergelijking: De verbrandingsreactie van een brandstof (zoals een koolwaterstof) met zuurstof produceert koolstofdioxide en water:
C_xh_y + (x + y/4) o2 → x CO2 + (y/2) H2O
2. Molaire massa: Zoek de molaire massa's van O2 (32 g/mol) en CO2 (44 g/mol).
3. stoichiometrie: Gebruik de gebalanceerde vergelijking om de molverhouding tussen O2 en CO2 te bepalen. In dit voorbeeld is de verhouding (x + y/4) mol O2 tot x mol CO2.
4. Berekening:
* Converteer de massa O2 in mol met behulp van zijn molaire massa.
* Pas de molverhouding van de gebalanceerde vergelijking toe om de mol CO2 geproduceerd te vinden.
Voorbeeld:
Laten we zeggen dat je 100 gram o2 hebt.
* mol O2: 100 g O2 / 32 g / mol =3,125 mol O2
* mol CO2: (Uitgaande van een eenvoudige reactie zoals CH4 + 2O2 → CO2 + 2H2O, waarbij de verhouding van O2 tot CO2 2:1) 3.125 mol O2 * is (1 mol CO2 / 2 mol O2) =1.5625 mol CO2
 Welke materialen komen in de chloroplast die gebruikte in lichtafhankelijke reacties?
Welke materialen komen in de chloroplast die gebruikte in lichtafhankelijke reacties?  Onderzoeksteam bereikt doorbraak in productie van veelgeprezen kankerbestrijdend medicijn
Onderzoeksteam bereikt doorbraak in productie van veelgeprezen kankerbestrijdend medicijn Welke van de volgende is een organisch molecuul?
Welke van de volgende is een organisch molecuul?  Zijn de BICEP2-resultaten ongeldig? Waarschijnlijk niet
Zijn de BICEP2-resultaten ongeldig? Waarschijnlijk niet  Hoe Lucas Reagent te maken
Hoe Lucas Reagent te maken
 Nieuw onderzoek roept op tot de bescherming van Britse kwelders
Nieuw onderzoek roept op tot de bescherming van Britse kwelders  Luchtfoto's laten zien dat tientallen jaren van bosgroei in de uitlopers is weggevaagd als gevolg van de extreme droogte in Californië
Luchtfoto's laten zien dat tientallen jaren van bosgroei in de uitlopers is weggevaagd als gevolg van de extreme droogte in Californië  Nieuw gebruik van navigatiesysteem bespaart kostbaar water
Nieuw gebruik van navigatiesysteem bespaart kostbaar water Welke zaden zullen het snelst ontkiemen voor een Science Fair-project?
Welke zaden zullen het snelst ontkiemen voor een Science Fair-project?  Antibiotica gevonden in sommige rivieren ter wereld overschrijden veilige niveaus, wereldwijde studie vindt
Antibiotica gevonden in sommige rivieren ter wereld overschrijden veilige niveaus, wereldwijde studie vindt
Hoofdlijnen
- Wat zijn twee kenmerken van mRNA in eukaryoten?
- Visresten kunnen grondstoffentekorten compenseren en tegelijkertijd onze gezondheid verbeteren
- De verborgen architect:hoe kernen de ogen en hersenen organiseren
- Leuke wasberen zijn superleerlingen en waarschijnlijk criminele meesterbreinen uit de vuilnisbak
- Onderzoek onthult inzichten in de evolutie van eiwitten
- Waar staat MASH in de wetenschap voor?
- Welk niveau van lichaamsorganisatie vertegenwoordigt het verteringspad?
- Welke vroege vorm van een organisme waaruit latere vormen dalen?
- Was Tricia de olifant gelukkig? Experts bespreken de ethiek van het in gevangenschap houden van zulke grote, rondzwervende wezens
- Bestrijding van kunstmatige trilhaartjes met magnetische velden en licht

- Door UA uitgevonden zonnebrandcrème in licentie gegeven aan toonaangevende leverancier van aloë vera

- Batterijen verborgen laag onthuld
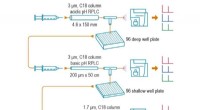
- Verbeterde eiwitanalyse kan vroege ziektedetectie helpen
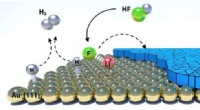
- Alternatief voor stikstof:Zuurstofplasma kan de eigenschappen van elektrodematerialen verbeteren
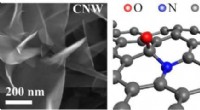
 Wat zijn de belangrijkste niet -hernieuwbare en renwabele energiebronnen?
Wat zijn de belangrijkste niet -hernieuwbare en renwabele energiebronnen?  Wat is de chemische formule van het Hinsberg-reagens?
Wat is de chemische formule van het Hinsberg-reagens?  Onderzoekers:Schaf huwelijksvoltrekking af als vereiste voor burgerschap
Onderzoekers:Schaf huwelijksvoltrekking af als vereiste voor burgerschap Hoe we de locatie van een snelle radio-uitbarsting in een ver sterrenstelsel naderden, ver weg
Hoe we de locatie van een snelle radio-uitbarsting in een ver sterrenstelsel naderden, ver weg Rook uit derde hand en de risico's ervan onder de loep
Rook uit derde hand en de risico's ervan onder de loep Marcheren voor verandering:Womens March 2017 kreeg overwegend positieve online steun
Marcheren voor verandering:Womens March 2017 kreeg overwegend positieve online steun Amazon-medewerkers staken in Spanje en Duitsland (update)
Amazon-medewerkers staken in Spanje en Duitsland (update) Over 30 jaar verdwenen? Het dorp in Wales in het vizier van klimaatverandering
Over 30 jaar verdwenen? Het dorp in Wales in het vizier van klimaatverandering
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

