
Wetenschap
Waarom wordt rode kool gebruikt als kleine pH -indicator?
* Anthocyanines veranderen van kleur met pH: Anthocyanen zijn in water oplosbare pigmenten die in veel planten worden gevonden, waaronder rode kool. Hun kleur verandert afhankelijk van de zuurgraad (pH) van hun omgeving.
* Een breed scala aan kleurveranderingen: In zure oplossingen (lage pH) worden anthocyanen rood of roze. Naarmate de oplossing eenvoudiger wordt (hoge pH), worden ze paars, blauw of groen. Dit biedt een visuele indicator van het pH -bereik.
* gemakkelijk te gebruiken: Rode kool is direct beschikbaar en gemakkelijk om het anthocyaninepigment te extraheren. Het eenvoudig koken van rode koolbladeren in water produceert een oplossing die kan worden gebruikt als pH -indicator.
Hier is hoe het werkt:
1. Extractie: Koken rode kool brengt de anthocyaninen uit de plantencellen in het water.
2. Kleurverandering: Wanneer u deze oplossing aan een stof toevoegt, reageren de anthocyaninen met de aanwezige waterstofionen (H+). Hoe hoger de concentratie van H+ (lagere pH), hoe meer rood de oplossing wordt. Omgekeerd leiden lagere concentraties van H+ (hogere pH) tot een meer blauwe of groene kleur.
Andere voordelen van het gebruik van rode kool als pH -indicator:
* natuurlijk: Het is een niet-toxisch en milieuvriendelijk alternatief voor synthetische pH-indicatoren.
* kosteneffectief: Rode kool is goedkoop en direct beschikbaar.
* educatief: Het is een leuke en boeiende manier om les te geven over pH en zuur-base chemie.
Red Cabbage biedt dus een eenvoudige, visuele en effectieve manier om het concept van pH en het effect ervan op de kleur van oplossingen te begrijpen.
 Ontbossing gekoppeld aan palmolieproductie maakt Indonesië warmer
Ontbossing gekoppeld aan palmolieproductie maakt Indonesië warmer Hoe zorgen hogere golven voor meer ijswolken? Onderzoeksexpeditie in de arctische zee legt uit
Hoe zorgen hogere golven voor meer ijswolken? Onderzoeksexpeditie in de arctische zee legt uit Wat is het oppervlak in planten?
Wat is het oppervlak in planten?  Geheimen van de grootste koolstofput op aarde onthuld door synchrotron-onderzoek
Geheimen van de grootste koolstofput op aarde onthuld door synchrotron-onderzoek Vraag en antwoord:Wat betekent het verlaten van de klimaatovereenkomst van Parijs voor het bedrijfsleven?
Vraag en antwoord:Wat betekent het verlaten van de klimaatovereenkomst van Parijs voor het bedrijfsleven?
Hoofdlijnen
- Hoe kan computertechnologie de toekomst van gensynthese voorspellen?
- Lichamelijke afbraak uitgelegd:hoe celdifferentiatiepatronen de somatische evolutie onderdrukken
- Welk enzym gebruiken wetenschappers om genen uit strengen te snijden als DNA?
- Wat zou er gebeuren als de micro -organismen uit de voedselketen werden verwijderd?
- Onderzoek lost de puzzel op waarom de hommel zo goed kan vliegen
- Planten kunnen kiezen tussen alternatieve reacties op concurrentie
- Zijn het alleen bijen die bestuiven?
- De kristalstructuur laat zien hoe motoreiwit werkt
- Doorbraak laat zien hoe DNA wordt 'bewerkt' om genetische ziekten te corrigeren
- Nieuwe topologische materialen kunnen meerdere elektrische eigenschappen hebben

- Onderzoekers smeden nieuwe rekenhulpmiddelen om nauwkeuriger voorspellingen te doen van eiwitstructuren

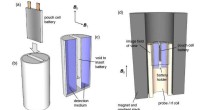
- Chemici ontwikkelen MRI-achtige techniek om te detecteren wat er aan de hand is met batterijen
- Moleculaire schakelaar zal de ontwikkeling van baanbrekende elektro-optische apparaten vergemakkelijken

- Samenwerking vormt de strategie voor het vasthouden van extracellulaire blaasjes
 Hoe emoties het werkleven vormgeven
Hoe emoties het werkleven vormgeven Wat is de connotatieve betekenis van steen?
Wat is de connotatieve betekenis van steen?  Hubble ziet wervelingen van vormende sterren
Hubble ziet wervelingen van vormende sterren Wat is Caster Metal?
Wat is Caster Metal?  Wetenschappers beschrijven het meest complete fossiel uit de vroege stadia van de evolutie van de uil
Wetenschappers beschrijven het meest complete fossiel uit de vroege stadia van de evolutie van de uil Zullen alternatieve brandstoffen de mondiale maïsvoorraden uitputten?
Zullen alternatieve brandstoffen de mondiale maïsvoorraden uitputten?  Klimaatverandering zal waarschijnlijk donkere tropische bossen veroorzaken, onderzoekers zeggen:
Klimaatverandering zal waarschijnlijk donkere tropische bossen veroorzaken, onderzoekers zeggen: Ga er niet vanuit dat online studenten meer kans hebben om vals te spelen. Het bewijs is duister
Ga er niet vanuit dat online studenten meer kans hebben om vals te spelen. Het bewijs is duister
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

