
Wetenschap
Wat voor soort reactie treedt op wanneer water en een metaaloxide reageren om hydroxide te vormen?
Hier is een uitsplitsing:
* metaaloxide is een verbinding die een metaalkation en een oxide -anion (o²⁻) bevat.
* Water is een polair molecuul met een enigszins positieve waterstofzijde en een enigszins negatieve zuurstofzijde.
* hydroxide is een verbinding die een metalen kation en een hydroxide -anion bevat (OH⁻).
De reactie:
De positieve waterstofzijde van water trekt het negatieve oxide -ion in het metaaloxide aan, terwijl de negatieve zuurstofzijde van water het positieve metaalion aantrekt. Dit resulteert in een dubbele verplaatsing, waarbij het oxide -ion van het metaaloxide combineert met een waterstofion van water om een hydroxide -ion (OH⁻) te vormen, en het metaalion van het metaaloxide combineert met het hydroxide -ion om het metaalhydroxide te vormen.
Algemene vergelijking:
Metaaloxide + water → metaalhydroxide
Voorbeeld:
Natriumoxide (Na₂o) reageert met water om natriumhydroxide (NaOH) te vormen:
Na₂o + H₂o → 2naOH
Deze reactie wordt ook geclassificeerd als een exotherme reactie , terwijl het warmte vrijgeeft.
Opmerking: Niet alle metaaloxiden reageren met water om hydroxiden te vormen. De reactiviteit hangt af van de positie van het metaal in de reactiviteitsreeks. Oxiden van alkali -metalen en alkalische aardmetalen zijn bijvoorbeeld over het algemeen reactief met water, terwijl overgangsmetaaloxiden over het algemeen minder reactief zijn.
 Welke moleculen bevatten een niet-polaire covelente binding?
Welke moleculen bevatten een niet-polaire covelente binding?  Hoe krijgt verf een positieve lading wanneer het spuitmondstuk verlaat?
Hoe krijgt verf een positieve lading wanneer het spuitmondstuk verlaat?  Moleculaire tweak verbetert de prestaties van organische zonnecellen
Moleculaire tweak verbetert de prestaties van organische zonnecellen Met deze techniek kunnen onderzoekers onderzoeken hoe materialen zich op atomair niveau binden
Met deze techniek kunnen onderzoekers onderzoeken hoe materialen zich op atomair niveau binden  Wetenschappers ontwerpen nieuwe metabole technologie om wetenschappelijke gegevens voor iedereen te openen
Wetenschappers ontwerpen nieuwe metabole technologie om wetenschappelijke gegevens voor iedereen te openen
 Beschermen we rivieren en beken echt tegen vervuiling? Het is moeilijk te zeggen, en dat is een probleem
Beschermen we rivieren en beken echt tegen vervuiling? Het is moeilijk te zeggen, en dat is een probleem NASA kijkt naar hardnekkige overblijfselen van ex-tropische cycloon Iris
NASA kijkt naar hardnekkige overblijfselen van ex-tropische cycloon Iris Onderzoekers schatten 10, 000 ton plastic komt elk jaar de Grote Meren binnen
Onderzoekers schatten 10, 000 ton plastic komt elk jaar de Grote Meren binnen De voordelen van bitter zijn:hoe de evolutie van de cranberry er een Thanksgiving-hoofdbestanddeel van maakte
De voordelen van bitter zijn:hoe de evolutie van de cranberry er een Thanksgiving-hoofdbestanddeel van maakte  Vulkanische gevarenscenario's:Mount Taranaki, Nieuw-Zeeland
Vulkanische gevarenscenario's:Mount Taranaki, Nieuw-Zeeland
Hoofdlijnen
- Wat scheidt de cel van zijn omgeving en selecteert wat kan invoeren?
- Wat gebeurt er volgens de wet van segregatie van Mendel tijdens meiose?
- Wat voor soort aseksuele reproductie wordt voortplanting zonder dat hun eieren worden bevrucht?
- Hoe de varkensgriep werkt
- Wat eet Ambeoa?
- Op welke vier manieren kunnen leden van de soort samenwerken zijn?
- Welk type organismen bevinden zich op het eerste trofische niveau?
- Het team van Rensselaer laat zien hoe je ruwe overheidsdata analyseert
- Onderzoekers beschrijven hoe cellen het afval buiten zetten om ziekten te voorkomen
- Onderzoekers ontwikkelen goedkope, drop-on-demand printtechniek

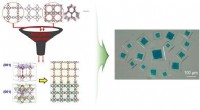
- Algoritme identificeert optimale paren voor het samenstellen van metaal-organische raamwerken
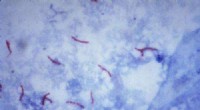
- Kleine robot kan game-changer zijn in de strijd tegen tuberculose
- Platinavrije katalysatoren kunnen goedkopere waterstofbrandstofcellen maken

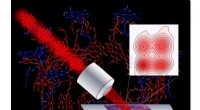
- Onderzoekers ontwikkelen microscoop om lichtenergiestroom in fotosynthetische cellen te volgen
 Wat betekent bodemafbeelding?
Wat betekent bodemafbeelding?  Hoe de perimeter van een kwadrant te vinden
Hoe de perimeter van een kwadrant te vinden  Duitse officieren van justitie vallen VW in verband met uitstoot van kooldioxide
Duitse officieren van justitie vallen VW in verband met uitstoot van kooldioxide De nieuwe generatie Starlink-satellieten blijft boven de geaccepteerde helderheidsdrempel
De nieuwe generatie Starlink-satellieten blijft boven de geaccepteerde helderheidsdrempel meer wapens, pandemische stress en een legitimiteitscrisis van de politie creëerden perfecte omstandigheden voor een piek in moordzaken in 2020
meer wapens, pandemische stress en een legitimiteitscrisis van de politie creëerden perfecte omstandigheden voor een piek in moordzaken in 2020 Astronomen detecteren 22 nieuwe catastrofale variabelen in bolvormige sterrenhoop 47 Tucanae
Astronomen detecteren 22 nieuwe catastrofale variabelen in bolvormige sterrenhoop 47 Tucanae Wat voor soort opgeloste deeltjes zijn aanwezig in een oplossing een ionische verbinding?
Wat voor soort opgeloste deeltjes zijn aanwezig in een oplossing een ionische verbinding?  Kenyas Lake Turkana op Werelderfgoedlijst van gevaren
Kenyas Lake Turkana op Werelderfgoedlijst van gevaren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

