
Wetenschap
Welke ionen heeft dezelfde elektronenconfiguratie als Argon AR?
1. Begrijp Argon's elektronenconfiguratie
Argon (AR) heeft een atoomnummer van 18, wat betekent dat het 18 protonen en 18 elektronen heeft. De elektronenconfiguratie is:
1S² 2S² 2P⁶ 3S² 3P⁶
2. Identificeer ionen met hetzelfde aantal elektronen
Om dezelfde elektronenconfiguratie als argon te hebben, moet een ion ook 18 elektronen hebben. Dit kan worden bereikt door:
* Elektronen verkrijgen: Anionen (negatief geladen ionen) worden gevormd door elektronen te winnen.
* Elektronen verliezen: Kationen (positief geladen ionen) worden gevormd door elektronen te verliezen.
3. Bepaal de ionen
Hier zijn de ionen met dezelfde elektronenconfiguratie als argon:
* k⁺ (kaliumion): Kalium (K) heeft 19 elektronen. Door één elektron te verliezen, wordt het K⁺ met 18 elektronen.
* ca²⁺ (calciumion): Calcium (CA) heeft 20 elektronen. Door twee elektronen te verliezen, wordt het ca²⁺ met 18 elektronen.
* CL⁻ (chloride -ion): Chloor (CL) heeft 17 elektronen. Door één elektron te winnen, wordt het Cl⁻ met 18 elektronen.
* s²⁻ (sulfide -ion): Zwavel (s) heeft 16 elektronen. Door twee elektronen te winnen, wordt het S²⁻ met 18 elektronen.
Samenvattend: De ionen k⁺, ca²⁺, cl⁻ en s²⁻ hebben allemaal dezelfde elektronenconfiguratie als argon. Dit komt omdat ze allemaal 18 elektronen hebben, net als Argon.
 Onderzoekers ontwikkelen op neuronen geïnspireerd, hoogwaardig telechelisch polymeer
Onderzoekers ontwikkelen op neuronen geïnspireerd, hoogwaardig telechelisch polymeer Elk element heeft zijn eigen atoomnummer waar het van is?
Elk element heeft zijn eigen atoomnummer waar het van is?  Team ontwikkelt productieproces voor biobrandstof in samenwerking met Noord-Amerikaanse onderzoekers
Team ontwikkelt productieproces voor biobrandstof in samenwerking met Noord-Amerikaanse onderzoekers Computationeel onderzoek onthult hoe Ebola-nucleocapside stabiliseert
Computationeel onderzoek onthult hoe Ebola-nucleocapside stabiliseert  Marihuana hoe werkt
Marihuana hoe werkt
 Informatie over de Cormorant Bird
Informatie over de Cormorant Bird  Soorten dieren in het gematigde bos en struikgewas
Soorten dieren in het gematigde bos en struikgewas NASA volgt ex-tropische cycloon Esther boven Northern Territory
NASA volgt ex-tropische cycloon Esther boven Northern Territory Organische koolstof verbergt zich in sedimenten, zuurstof in de atmosfeer houden
Organische koolstof verbergt zich in sedimenten, zuurstof in de atmosfeer houden Hoe huisvestingsdiscriminatie de ongelijkheid op milieugebied beïnvloedt
Hoe huisvestingsdiscriminatie de ongelijkheid op milieugebied beïnvloedt
Hoofdlijnen
- Welke structuur zet voedsel om in onstabiele chemische energie door cellulaire ademhaling?
- Waar komt de zuurstof vandaan die je lichaam nodig heeft?
- Hoe Salmonella de zuuraanval van de macrofaag overleeft
- Wat is een biologische cayalyst?
- Is een virus niet-levend of levend?
- Raad eens wie? Gezichten van chimpansees onthullen familierelaties
- Papegaaien geven de voorkeur aan live videogesprekken boven het bekijken van vooraf opgenomen video's van andere vogels
- Hoe zeer resistente schimmelsoorten ontstaan
- Maki-darm is niet één ecosysteem, het zijn er veel
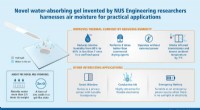
- Nieuwe hydrogel benut luchtvochtigheid voor praktische toepassingen
- Massaspectrometrietechniek helpt bij het identificeren van vervalste manuscripten van Robert Burns

- Programmeerbare structuren van de printer

- Kunstmatige bio-geïnspireerde membranen voor waterfiltratie
- Een rechterhand in een linkshandige want passen
 Wat gebeurt er als een vogel een vliegtuig raakt?
Wat gebeurt er als een vogel een vliegtuig raakt?  Kinetic Energy Experiments voor kinderen
Kinetic Energy Experiments voor kinderen  Hoe zee-ijsafwijkingen in de Barentsz-Kara Zee worden gemoduleerd door het 'warme Arctische-koude Eurazië'-patroon
Hoe zee-ijsafwijkingen in de Barentsz-Kara Zee worden gemoduleerd door het 'warme Arctische-koude Eurazië'-patroon  SoftBank onthult investeringsfonds om AI-revolutie te stimuleren
SoftBank onthult investeringsfonds om AI-revolutie te stimuleren Hoe de opname van watermoleculen in gelaagde materialen het ionenopslagvermogen beïnvloedt
Hoe de opname van watermoleculen in gelaagde materialen het ionenopslagvermogen beïnvloedt  Stijgt een ballon met helium hoger dan één met zuurstof?
Stijgt een ballon met helium hoger dan één met zuurstof?  Isotopen gebruiken om het binnendringen van zout water in het grondwater van Rottnest Island te begrijpen
Isotopen gebruiken om het binnendringen van zout water in het grondwater van Rottnest Island te begrijpen Expert legt de inhoud uit van de CHIPS and Science Act, de halfgeleiderwet
Expert legt de inhoud uit van de CHIPS and Science Act, de halfgeleiderwet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

