
Wetenschap
Wat zijn polariseerbare anionen?
polariseerbare anionen:een nadere blik
Polariseerbare anionen zijn negatief geladen ionen die hun elektronenwolk kunnen vervormen door de aanwezigheid van een positieve lading in de buurt. Deze vervorming, bekend als polarisatie , beïnvloedt de reactiviteit en eigenschappen van het anion.
Key -kenmerken van polariseerbare anionen:
* Groot formaat: Grotere anionen hebben meer diffuse elektronenwolken, waardoor ze gevoeliger zijn voor vervorming.
* Hoge ladingsdichtheid: Anionen met een hogere ladingsdichtheid (meer lading geconcentreerd in een kleinere ruimte) zijn meer polariseerbaar.
* Zwak gebonden elektronen: Anionen met elektronen die zwak worden vastgehouden door de kern zijn gemakkelijker vervormd.
Voorbeelden van polariseerbare anionen:
* jodide-ion (i-) :Jodide is een groot anion met een relatief diffuse elektronenwolk, waardoor het zeer polariseerbaar is.
* sulfide-ion (S2-) :Sulfide heeft een hoge ladingsdichtheid en is ook zeer polariseerbaar.
* bromide-ion (Br-) :Net als jodide is bromide een groot anion met een diffuse elektronenwolk.
Impact van polarisatie op anioneigenschappen:
* Reactiviteit: Polariseerbare anionen zijn reactiever dan hun minder polariseerbare tegenhangers. Dit komt omdat de vervormde elektronenwolk tijdelijke dipolen creëert die kunnen interageren met andere moleculen of ionen, wat leidt tot verhoogde reactiviteit.
* Oplosbaarheid: Polarisatie kan de oplosbaarheid beïnvloeden. Zeer polariseerbare anionen zijn bijvoorbeeld vaak minder oplosbaar in polaire oplosmiddelen zoals water.
* Coördinatiechemie: Polariseerbare anionen worden vaak gevonden als liganden in coördinatiecomplexen, waar ze interageren met metaalionen via hun gepolariseerde elektronenwolken.
Voorbeelden van hoe polarisatie de reacties beïnvloedt:
* SN2 -reacties: Polariseerbare anionen zijn goede nucleofielen in SN2 -reacties, omdat hun vervormde elektronenwolken het elektrofiele koolstofcentrum gemakkelijk kunnen aanvallen.
* Vorming van covalente bindingen: Polariseerbare anionen kunnen sterkere covalente bindingen vormen met elektropositieve atomen als gevolg van de verbeterde elektronenuitwisseling veroorzaakt door polarisatie.
* stabilisatie van tussenproducten: Polarisatie kan reactietussenproducten stabiliseren door lading te verspreiden en de elektronendichtheid in specifieke gebieden te verminderen.
Inzicht in het concept van polariseerbare anionen is cruciaal voor het voorspellen van het gedrag van chemische reacties en het begrijpen van de eigenschappen van verschillende chemische verbindingen.
 Ontdekking van spiraalvormige moleculaire lijm
Ontdekking van spiraalvormige moleculaire lijm Waarom zit er maar één zuurstofion in magnesiumoxide?
Waarom zit er maar één zuurstofion in magnesiumoxide?  Wat is het atomaire massagetal van een isotoop met 5 en 6 neutronen?
Wat is het atomaire massagetal van een isotoop met 5 en 6 neutronen?  Next-gen membranen voor het afvangen van koolstof
Next-gen membranen voor het afvangen van koolstof Beeldvorming van opeenvolgende potentiaalverdelingsveranderingen in elektroden tijdens laden/ontladen
Beeldvorming van opeenvolgende potentiaalverdelingsveranderingen in elektroden tijdens laden/ontladen
Hoofdlijnen
- Leg 2 manieren uit waarop technologie wordt gebruikt op het gebied van genetica?
- Hoe converteert ADP naar ATP?
- Onderzoek onderzoekt hoe druivenplagen bessen opsnuiven
- Wat zijn de biomoleculen van koolhydraten?
- Onderzoekers vergroten het inzicht in waarom celonderdelen er zo uitzien zoals ze eruit zien
- De morfologie van algen
- Welk enzym is betrokken bij RNA -verlenging?
- Cytoplasma bacteriecellen
- Trucs voor het onthouden van dieren Phylum
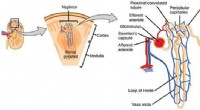
- Apparaat om de ontdekking van geneesmiddelen voor nierziekten te versnellen
- Onderzoekers creëren aerogels met vormgeheugen met rubberachtige elasticiteit

- Dankzij de techniek voor het bewerken van genen kunnen zijderupsen spinnenzijde produceren

- Kunstmatige antimicrobiële peptiden kunnen helpen om resistente bacteriën te overwinnen
- Weggegooide sigarettenpeuken - het volgende hoogwaardige waterstofopslagmateriaal?

 Om te slagen in een AI-wereld, studenten moeten de menselijke eigenschappen van schrijven leren
Om te slagen in een AI-wereld, studenten moeten de menselijke eigenschappen van schrijven leren Lava stroomde 9,3 kilometer per uur per uur de lava bereikte de zee in 3 uur hoeveel zijn er uit de bron van lava?
Lava stroomde 9,3 kilometer per uur per uur de lava bereikte de zee in 3 uur hoeveel zijn er uit de bron van lava?  De vaste aarde ademt
De vaste aarde ademt Als Google in Lyft investeert, wat betekent dat dan voor Uber?
Als Google in Lyft investeert, wat betekent dat dan voor Uber?  Welk type fouten worden geassocieerd met bergen van foutblokken?
Welk type fouten worden geassocieerd met bergen van foutblokken?  Wetenschappers ontwikkelen de volgende generatie van reservoir computing
Wetenschappers ontwikkelen de volgende generatie van reservoir computing Wat is het beste om de emissie van koolstofdioxide te verminderen?
Wat is het beste om de emissie van koolstofdioxide te verminderen?  Je doel opgeven? Lees dit eerst
Je doel opgeven? Lees dit eerst
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

