
Wetenschap
Als een onvoldoende hoeveelheid van een vloeistof onbekend was gebruikt, hoe zou dit de waarde -experimentele molaire massa beïnvloeden?
* Molaire massaberekening: Molaire massa wordt berekend door de massa van de stof te delen door het aantal mol.
* onvoldoende vloeistof: Het gebruik van minder vloeistof betekent dat u een kleinere massa hebt. Omdat het aantal mol hetzelfde blijft (uitgaande van de concentratie constant), leidt een kleinere massa tot een grotere berekende molaire massa.
Voorbeeld:
Stel je voor dat je de molaire massa van een vloeistof moet meten. U moet 10 gram vloeistof gebruiken, maar u gebruikt per ongeluk slechts 5 gram.
* Correcte berekening: (10 g / mol) =molaire massa
* Onjuiste berekening: (5 g / mol) =molaire massa (die het dubbele zal zijn van de juiste waarde)
Samenvattend: Het gebruik van te weinig vloeistof leidt tot een onderschatting van de massa, wat resulteert in een overschatting van de molaire massa.
 Wat zijn twee manieren waarop de snelheid van een chemische reactie kan worden verhoogd als beide reactanten waterige oplossingen kunnen reactanten?
Wat zijn twee manieren waarop de snelheid van een chemische reactie kan worden verhoogd als beide reactanten waterige oplossingen kunnen reactanten?  Hoe een proteaseremmer te bereiden Cocktail
Hoe een proteaseremmer te bereiden Cocktail Een hydrogel die stevig hecht aan kraakbeen en meniscus
Een hydrogel die stevig hecht aan kraakbeen en meniscus Wat hebben cohesie, oppervlaktespanning en adhesie allemaal gemeen met betrekking tot water?
Wat hebben cohesie, oppervlaktespanning en adhesie allemaal gemeen met betrekking tot water?  Moleculair ontwerpen van polymeernetwerken om geluidsdemping te beheersen
Moleculair ontwerpen van polymeernetwerken om geluidsdemping te beheersen
 NASA ziet Damrey sterker worden tot tyfoon
NASA ziet Damrey sterker worden tot tyfoon Klimaatverandering kan leiden tot grotere atmosferische rivieren
Klimaatverandering kan leiden tot grotere atmosferische rivieren Nieuwe aanpak van supergladde verpakkingen is bedoeld om voedselverspilling te verminderen
Nieuwe aanpak van supergladde verpakkingen is bedoeld om voedselverspilling te verminderen 'Een dikke dunk?' Het prehistorische zeemonster van Cleveland was mogelijk korter en steviger dan ooit werd gedacht
'Een dikke dunk?' Het prehistorische zeemonster van Cleveland was mogelijk korter en steviger dan ooit werd gedacht  Veranderingen in het post-Sovjet-voedselsysteem leidden tot reductie van broeikasgassen
Veranderingen in het post-Sovjet-voedselsysteem leidden tot reductie van broeikasgassen
Hoofdlijnen
- Hoe haarverf bijdraagt aan het behoud van de Australische zeeleeuwenpopulatie
- Welke consumenten voeden zich met algen?
- Wat is een voorbeeld van iets dat de basisstructuren een levend organisme mist en homeostase niet kan metaboliseren of onderhouden?
- Trias-exemplaar dat een eeuw na de ontdekking ervan vroeg verwant is aan pterosauriërs
- Wie heeft sportdranken uitgevonden?
- Wat is de werking van het celmembraan van alle organismen?
- Vier soorten limu krijgen Hawaiiaanse namen
- Een nieuwe rol voor de eiwitfamilie zou een pad kunnen bieden voor de manier waarop gewaseigenschappen worden gewijzigd
- Welke materialen worden opgeslagen in planten?
- Enzym ontdekt in de darm kan leiden tot nieuwe biomarker voor ziekten
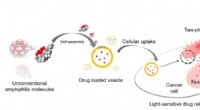
- Nieuwe technologie voor de levering van geneesmiddelen tegen kanker op aanvraag
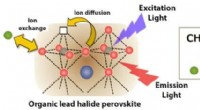
- Succes bij het beheersen van de samenstelling van perovskitionen maakt de weg vrij voor apparaattoepassingen
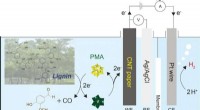
- Een nieuw biobrandstofsysteem voor waterstofproductie uit biomassa
- DNA-gebaseerd materiaal met afstembare eigenschappen

 "Wat gebeurt er?" Twitter wil het weten
"Wat gebeurt er?" Twitter wil het weten  Een ballon met een gewicht van 1 N hangt in de lucht en zweeft niet omhoog of omlaag. Hoeveel drijvende kracht werkt er op?
Een ballon met een gewicht van 1 N hangt in de lucht en zweeft niet omhoog of omlaag. Hoeveel drijvende kracht werkt er op?  Studie onthult nieuwe inzichten in hoe hybride perovskiet-zonnecellen werken
Studie onthult nieuwe inzichten in hoe hybride perovskiet-zonnecellen werken Behouden sneeuwvlokken die zich in een wolk vormen massa?
Behouden sneeuwvlokken die zich in een wolk vormen massa?  Stikstofstoot heeft sargassum veranderd in 's werelds grootste schadelijke algenbloei
Stikstofstoot heeft sargassum veranderd in 's werelds grootste schadelijke algenbloei Strontium nitraat- en natriumsulfide -participatiereacties?
Strontium nitraat- en natriumsulfide -participatiereacties?  Welke voedingsstof wordt gevonden in de wortels van planten?
Welke voedingsstof wordt gevonden in de wortels van planten?  Nieuw licht werpen op het uitwerpen van zwarte gaten
Nieuw licht werpen op het uitwerpen van zwarte gaten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

