
Wetenschap
Heeft een katalysator invloed op de enthalpie van de reactie?
Dit is waarom:
* Enthalpy Change is een statusfunctie: Dit betekent dat het alleen afhangt van de initiële en uiteindelijke toestanden van het systeem, niet op het genomen pad.
* katalysatoren veranderen het pad: Een katalysator biedt een alternatieve route met een lagere activeringsenergie, waardoor de reactie wordt versneld. Het verandert echter niet het algemene energieverschil tussen reactanten en producten.
* Energiebesparing: De totale energie van het systeem blijft constant, zelfs met een katalysator. De energie die wordt vrijgegeven of geabsorbeerd tijdens een reactie (enthalpieverandering) is onafhankelijk van de katalysator.
Denk er zo aan: Stel je een bal voor die over een heuvel rolt. De katalysator is als het bouwen van een helling, waardoor het voor de bal gemakkelijker wordt om de bodem te bereiken. De helling verandert niet het hoogteverschil tussen de boven- en onderkant van de heuvel (enthalpieverandering), het maakt de reis gewoon sneller.
Samenvattend: Katalysatoren beïnvloeden de snelheid van een reactie, maar ze veranderen de enthalpieverandering (vrijgegeven of geabsorbeerde warmte niet) geassocieerd met de reactie.
 Onderzoekers evalueren het potentieel van perovskiet-zonnecellen voor ruimtetoepassingen
Onderzoekers evalueren het potentieel van perovskiet-zonnecellen voor ruimtetoepassingen CryoEM-onderzoek legt opioïde-signalering vast
CryoEM-onderzoek legt opioïde-signalering vast Hoe te vinden hoeveel Mollen in een samenstelling zitten
Hoe te vinden hoeveel Mollen in een samenstelling zitten  Hoe wordt de formule van een verbinding bepaald?
Hoe wordt de formule van een verbinding bepaald?  Geen boter of eieren meer? Hier is de wetenschap achter vervangende ingrediënten
Geen boter of eieren meer? Hier is de wetenschap achter vervangende ingrediënten
Hoofdlijnen
- Waarom gebruiken wetenschappers Bat Box?
- Waarom de menselijke stem zo veelzijdig is
- Maakt Botox je gelukkiger als het je frons wegneemt?
- Onderzoeksartikelen werpen licht op een decennium lang stamcelmysterie
- Bijtkrachtonderzoek onthult dinosaurus-etende kikker
- Wat is de functie van zaadwortel in dicot?
- Simpele microscoopexperimenten
- Zijn eicellen bij ouder wordende primaten beschermd tegen mutaties?
- Wat is een spoel van mitochondria?
- 3D-beeldvorming van oppervlaktechemie in opsluiting

- Machine-learning maakt een voorheen ongeziene kijk op polymeren die nuttig zijn op biomedisch gebied mogelijk

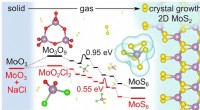
- Bestudeer details waarom 2D-vorming van molybdeendisulfide een snelheidsboost krijgt van zout
- Onderzoek naar aluminiumlegeringen kan bemande ruimtemissies ten goede komen

- Water, overal water - en het is vreemder dan je denkt

 Wat is de enthalpie van water bij kamertemperatuur?
Wat is de enthalpie van water bij kamertemperatuur?  Wat worden enzymen overwogen?
Wat worden enzymen overwogen?  Vreemd fruit:hoe Billie Holidays uitvoering van het anti-lynchlied het zwarte bewustzijn politiseerde
Vreemd fruit:hoe Billie Holidays uitvoering van het anti-lynchlied het zwarte bewustzijn politiseerde  Hoe krijgt bloed zuurstof?
Hoe krijgt bloed zuurstof?  Wat is de chemische formule voor zeoliet?
Wat is de chemische formule voor zeoliet?  Eerste momentopname van exciton-polariton condensatieproces
Eerste momentopname van exciton-polariton condensatieproces Nieuwe inzichten in hoe celmembranen de ontwikkeling van peptiden bij de ziekte van Alzheimer beïnvloeden
Nieuwe inzichten in hoe celmembranen de ontwikkeling van peptiden bij de ziekte van Alzheimer beïnvloeden  Probeert u geld te besparen? Uit onderzoek blijkt dat je contant moet betalen, nu het nog kan
Probeert u geld te besparen? Uit onderzoek blijkt dat je contant moet betalen, nu het nog kan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

