
Wetenschap
Waarom zijn ionische verbindingen oplosbaar in water maar niet in Keroscene -olie?
oplosbaarheid en polariteit
* water (h₂o): Water is een polaire molecuul. Dit betekent dat het een enigszins positief uiteinde heeft (de waterstofatomen) en een enigszins negatief uiteinde (het zuurstofatoom). Met deze polariteit kunnen watermoleculen sterk communiceren met de positieve en negatieve uiteinden van ionische verbindingen, ze uit elkaar trekken en oplost.
* kerosine: Kerosine is een mengsel van koolwaterstoffen, die nonpolar zijn moleculen. Niet -polaire moleculen hebben geen significante positieve of negatieve gebieden.
hoe het werkt
1. ionische verbindingen: Deze verbindingen worden gevormd door de elektrostatische aantrekkingskracht tussen positief geladen ionen (kationen) en negatief geladen ionen (anionen). Natriumchloride (NaCl) wordt bijvoorbeeld gevormd door Na+ en clionen.
2. De rol van het water: Wanneer een ionische verbinding in water wordt geplaatst, omringen de watermoleculen de ionen. De positieve uiteinden van watermoleculen (waterstofatomen) worden aangetrokken door de negatieve ionen en de negatieve uiteinden van watermoleculen (zuurstofatomen) worden aangetrokken door de positieve ionen. Deze elektrostatische interactie overwint de aantrekkingskracht tussen de ionen in het kristalrooster, waardoor de ionische verbinding oplost.
3 .'s rol van kerosine: Omdat kerosine niet -polair is, kan het niet effectief interageren met de geladen ionen van ionische verbindingen. De zwakke krachten tussen kerosine en de ionen zijn niet sterk genoeg om de aantrekkingskracht tussen de ionen zelf te overwinnen. Daarom zal de ionische verbinding niet oplossen.
Samenvattend
De sleutel tot het begrijpen van oplosbaarheid is "zoals oplost zoals." Polaire oplosmiddelen zoals water lossen polaire opgeloste stoffen op zoals ionische verbindingen, terwijl niet -polaire oplosmiddelen zoals kerosine niet -polaire opgeloste stoffen zoals koolwaterstoffen oplossen.
 Is het veranderen van een cent goud een chemische of fysische reactie?
Is het veranderen van een cent goud een chemische of fysische reactie?  Hoeveel atomen in molecuul ph3?
Hoeveel atomen in molecuul ph3?  Waarom gebruiken we een strook metaal op de plaats van de zekering?
Waarom gebruiken we een strook metaal op de plaats van de zekering?  Medische instrumenten worden gesteriliseerd onder de heetst mogelijke temperaturen, leg uit waarom ze in een autoclaaf een apparaat zijn dat in wezen snoepkoker en verwarmt Inst?
Medische instrumenten worden gesteriliseerd onder de heetst mogelijke temperaturen, leg uit waarom ze in een autoclaaf een apparaat zijn dat in wezen snoepkoker en verwarmt Inst?  Hoeveel liter zoutzuur zit er in 300 liter van een oplossing van 10 bij
Hoeveel liter zoutzuur zit er in 300 liter van een oplossing van 10 bij
 Eerdere overstromingsvoorspellingen om rampen in Japan te helpen voorkomen
Eerdere overstromingsvoorspellingen om rampen in Japan te helpen voorkomen Nucleaire oorlog kan grote El Nino veroorzaken en zeevruchten verminderen
Nucleaire oorlog kan grote El Nino veroorzaken en zeevruchten verminderen Antarctisch onderzoek toont aan dat de centrale ijskap stabiel is sinds mildere tijden
Antarctisch onderzoek toont aan dat de centrale ijskap stabiel is sinds mildere tijden Een nieuwe methode om oude aardbevingen te dateren
Een nieuwe methode om oude aardbevingen te dateren Studies in Bangladesh beschrijven hoe e-waste recycling werknemers blootstelt aan chemicaliën
Studies in Bangladesh beschrijven hoe e-waste recycling werknemers blootstelt aan chemicaliën
Hoofdlijnen
- Wat gebeurt er met een plant als de ademhalingssnelheid meer wordt dan de fotosynthese?
- Wat is de functie van vloeibaar wasmiddel bij genomische DNA-extractie?
- Eerder onbekende details van bladluizen tijdens de vlucht om bij te dragen aan een betere gewasveiligheid
- Wat is de functie van Steman?
- Wat concludeerde Thomas Hunt Morgan over de chromosomen van de fruitvlieg?
- Hoe bavianen gezonde gezinsgrenzen bewaren
- In welke organel komt cellulaire ademhaling op?
- Het ontrafelen van de mechanismen die de celgroei en -grootte regelen
- Bindweefselcellen die fagocytisch zijn?
- Onderzoekers bestuderen kooien van synthetische eiwitten

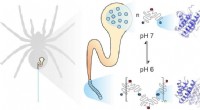
- Dynamiek van zijde-eiwitten is de sleutel tot uitstekende stabiliteit van spinzijde als biomateriaal
- Er komt iets slecht (ruikend) op deze manier - de wetenschap van stoffen en geuren

- Batterijen voor elektrische auto's inspireren veiliger, goedkopere manier om verbindingen te maken die in medicijnen worden gebruikt

- Nieuw multi-protondragercomplex als efficiënte protongeleider bij hoge temperaturen
 Is dit een bruine dwerg of een exoplaneet?
Is dit een bruine dwerg of een exoplaneet?  Hoe het geslacht van babyherten te bepalen
Hoe het geslacht van babyherten te bepalen Boek gaat over hoe landschapsontwerp waterproblemen helpt oplossen
Boek gaat over hoe landschapsontwerp waterproblemen helpt oplossen Hoe weet je dat er zwaartekracht is?
Hoe weet je dat er zwaartekracht is?  Studie vindt rioolbacteriën op de loer in sedimenten van de Hudson-rivier
Studie vindt rioolbacteriën op de loer in sedimenten van de Hudson-rivier Waarom zou poeder niet worden gebruikt in kokend water?
Waarom zou poeder niet worden gebruikt in kokend water?  Negatieve emissies, positieve economie
Negatieve emissies, positieve economie Thermische eigenschappen van grafeen kunnen helpen de opslagcapaciteit van magnetisch geheugen te vergroten
Thermische eigenschappen van grafeen kunnen helpen de opslagcapaciteit van magnetisch geheugen te vergroten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

