
Wetenschap
Waarom wordt molconcept gebruikt bij het balanceren van de chemische vergelijking?
Dit is hoe het molconcept een rol speelt in begrip en solliciteren evenwichtige chemische vergelijkingen:
* stoichiometrie: Zodra een chemische vergelijking in evenwicht is, vertegenwoordigen de coëfficiënten voor elk molecuul de molverhoudingen waarin reactanten reageren en producten worden gevormd. Bijvoorbeeld:
* 2 H₂ + O₂ → 2 H₂o
* Dit vertelt ons dat 2 mol waterstofgas reageert met 1 mol zuurstofgas om 2 mol water te produceren.
* Kwantitatieve berekeningen: Met het molconcept kunnen we de massa berekenen van reactanten en producten die betrokken zijn bij een reactie, of het volume van gassen, gebaseerd op de evenwichtige vergelijking. Dit is essentieel voor het uitvoeren van experimenten en het begrijpen van chemische processen.
Samenvattend is het molconcept essentieel voor het begrijpen van de kwantitatieve relaties in chemische reacties, maar het is niet direct betrokken bij het proces van het balanceren van vergelijkingen.
 Uitzonderlijke architectuur en de impact ervan op steden
Uitzonderlijke architectuur en de impact ervan op steden Na een bosbrand, attitudes over herstel variëren met gevoel van plaats en overtuigingen over brandecologie
Na een bosbrand, attitudes over herstel variëren met gevoel van plaats en overtuigingen over brandecologie Wat een goed wetenschapsbeursproject?
Wat een goed wetenschapsbeursproject?  De kracht van planten en hoe ze de manier waarop we leven veranderen
De kracht van planten en hoe ze de manier waarop we leven veranderen  NASA-studie vindt een verband tussen bosbranden en droogte
NASA-studie vindt een verband tussen bosbranden en droogte
Hoofdlijnen
- Relatie tussen één gen en polypeptide?
- Het plan om Catalina Island-herten te doden met behulp van scherpschutters in helikopters wordt tegengewerkt door LA County
- Hoe babyvissen een thuis vinden
- Zijn permanente veranderingen in een DNA die de nucleotidesequentie van een of meer genen beïnvloeden?
- Het grootste deel van onze hersenactiviteit is?
- Databank voor larvale vissen om de effecten van klimaatverandering op de visserij te laten zien
- Waarom papegaaien soms elkaars baby's adopteren (of doden)
- Waarom verspreidt ambrosia, een zeer allergene plant, zich zo snel?
- Wat is de behoefte aan centrifuge in DNA -isolatie?
- Chemie en informatica bundelen krachten om kunstmatige intelligentie toe te passen op chemische reacties

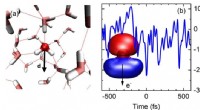
- Sterke velden en ultrasnelle bewegingen - hoe elektronen in vloeibaar water te genereren en te sturen?
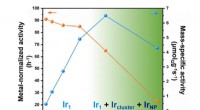
- Hoogbelastende atomair gedispergeerde Ir/MoC-katalysator voor hydrogeneringsreactie
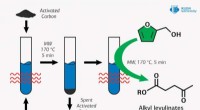
- Chemicus stelt nieuwe manier voor om de brandstofkwaliteit te verbeteren met behulp van microgolfstraling
- Een chemisch criterium voor het beoordelen van films

 Hoe verzamelen wetenschappers informatie?
Hoe verzamelen wetenschappers informatie?  Wat bepaalt de textuur van klastisch sedimentair gesteente, behalve de grootte en positie?
Wat bepaalt de textuur van klastisch sedimentair gesteente, behalve de grootte en positie?  Monitoring van de dynamiek van duizenden eiwitcomplexen tegelijk in intacte cellen
Monitoring van de dynamiek van duizenden eiwitcomplexen tegelijk in intacte cellen Afbeelding:Mount Sharp fotobommen Mars Curiosity rover
Afbeelding:Mount Sharp fotobommen Mars Curiosity rover Professor maakt visualisatietool voor klimaatgegevens die veranderingen in de atmosfeer in realtime kan onthullen
Professor maakt visualisatietool voor klimaatgegevens die veranderingen in de atmosfeer in realtime kan onthullen Onderzoek toont het belang van kustwaterkwaliteit aan voor recreatieve strandgebruikers
Onderzoek toont het belang van kustwaterkwaliteit aan voor recreatieve strandgebruikers Luisteraars kunnen zich aanpassen aan sprekerspecifieke akoestiek, studieprogramma's
Luisteraars kunnen zich aanpassen aan sprekerspecifieke akoestiek, studieprogramma's  Theoretisch perspectief op C-H/O-H activering door Cu-O in biologische en synthetische systemen
Theoretisch perspectief op C-H/O-H activering door Cu-O in biologische en synthetische systemen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

