
Wetenschap
Als een gas volume van 2,4L op 14,1 kPa bezet, wat zal de Occupy 84.6kpa?
Hier leest u hoe u dit probleem oplost met behulp van de wet van Boyle:
de wet van Boyle stelt dat het volume van een gas omgekeerd evenredig is met de druk, uitgaande van een constante temperatuur. Wiskundig:
P₁v₁ =p₂v₂
Waar:
* P₁ =Initiële druk
* V₁ =eerste volume
* P₂ =uiteindelijke druk
* V₂ =definitief volume
Gegeven:
* V₁ =2,4 l
* P₁ =14,1 kPa
* P₂ =84,6 kPa
Om te vinden: V₂
Oplossing:
1. Sluit de waarden aan op Boyle's Law -vergelijking:
(14,1 kPa) * (2.4 l) =(84,6 kPa) * V₂
2. Los op voor V₂:
V₂ =(14,1 kPa * 2.4 l) / 84,6 kPa
V₂ ≈ 0,4 l
Daarom zal het gas ongeveer 0,4 L bezetten bij een druk van 84,6 kPa.
 Wat betekent dit als een ijzeren spijker in een kopersulfaatoplossing wordt geplaatst en er een verdringingsreactie optreedt?
Wat betekent dit als een ijzeren spijker in een kopersulfaatoplossing wordt geplaatst en er een verdringingsreactie optreedt?  Welke term beschrijft een substantie die wordt gevormd door de combinatie van twee of meer elementen in bepaalde verhoudingen?
Welke term beschrijft een substantie die wordt gevormd door de combinatie van twee of meer elementen in bepaalde verhoudingen?  Waar staat de B voor in ultraviolet B?
Waar staat de B voor in ultraviolet B?  Hoe isotoop te vinden Mass
Hoe isotoop te vinden Mass Welke stoffen kunnen urenlang warmte vasthouden?
Welke stoffen kunnen urenlang warmte vasthouden?
 De tsunami in Alaska die golven veroorzaakte die zo hoog waren als de Space Needle van Seattle
De tsunami in Alaska die golven veroorzaakte die zo hoog waren als de Space Needle van Seattle S. Korea gaat 25% van de kolencentrales opschorten om vervuiling te bestrijden
S. Korea gaat 25% van de kolencentrales opschorten om vervuiling te bestrijden Hoe Morel-paddestoelen te jagen in Indiana
Hoe Morel-paddestoelen te jagen in Indiana Hogere temperatuur, zwaardere regen
Hogere temperatuur, zwaardere regen Steenkoralen beter bestand tegen klimaatverandering dan gedacht, studie vondsten
Steenkoralen beter bestand tegen klimaatverandering dan gedacht, studie vondsten
Hoofdlijnen
- Hoe eiwitten in gist communiceren om partners te vinden
- Angst voor de dood is van invloed op de manier waarop we stemmen
- Kunnen scholen vissen worden geïdentificeerd zonder menselijke tussenkomst?
- Het redden van Indonesische paradijsvogels dorp voor dorp
- Waarom slimme groei spelers in het systeem frustreert:studie
- Hoe worden planten genoemd die zaden hebben in gesloten schepen?
- Hoe worden fossielen gevormd in boomsap?
- How Do Living Things Grow?
- Albuminen zijn de plasma-eiwitten die verantwoordelijk zijn voor?
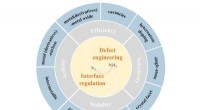
- Defect- en interface-engineering voor e-NRR onder omgevingsomstandigheden
- De gevoeligheid van COVID-tests meten met nieuw materiaal van NIST
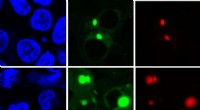
- Nieuwe methode gebruikt fluorescentie om ziekteverwekkende vormen van eiwitten te identificeren
- Onderzoekers ontwikkelen biohernieuwbare, biologisch afbreekbare kunststoffen

- Onderzoekers geven een nieuwe draai aan de oude techniek om beter absorberende materialen te ontwikkelen

 Californië heeft zijn klimaatdoel vroeg bereikt, maar de grootste bron van vervuiling blijft toenemen
Californië heeft zijn klimaatdoel vroeg bereikt, maar de grootste bron van vervuiling blijft toenemen Emissiedoelstellingen voor de transportsector kunnen niet worden gehaald met alleen aardgas
Emissiedoelstellingen voor de transportsector kunnen niet worden gehaald met alleen aardgas Canadese regering streeft naar koolstofneutraliteit tegen 2050
Canadese regering streeft naar koolstofneutraliteit tegen 2050 Nanodeeltjes die de levering van twee medicijnen spreiden, elimineren agressieve tumoren bij muizen
Nanodeeltjes die de levering van twee medicijnen spreiden, elimineren agressieve tumoren bij muizen China lanceert 3 astronauten op ruimtestationmissie van 6 maanden
China lanceert 3 astronauten op ruimtestationmissie van 6 maanden Hoeveel atomen 2NA2SO4?
Hoeveel atomen 2NA2SO4?  Amerikanen laten op Twitter zien dat ze hebben gestemd
Amerikanen laten op Twitter zien dat ze hebben gestemd  Brits klimaat:langere warme periodes, warmere zomerdagen
Brits klimaat:langere warme periodes, warmere zomerdagen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

