
Wetenschap
Wat zijn de gassen van eruit?
* Geen vaste vorm of volume: Gassen nemen de vorm en het volume van hun container aan.
* Compressibiliteit: Gassen kunnen worden gecomprimeerd, wat betekent dat hun volume kan worden verminderd door druk uit te oefenen.
* Expansibiliteit: Gassen breiden zich uit om de gehele beschikbare ruimte te vullen.
* Lage dichtheid: Gassen zijn over het algemeen veel minder dicht dan vaste stoffen of vloeistoffen.
* Hoge kinetische energie: Gasmoleculen hebben een hoge kinetische energie en bewegen snel in willekeurige richtingen.
* Zwakke intermoleculaire krachten: De aantrekkelijke krachten tussen gasmoleculen zijn zwak, waardoor ze vrij kunnen bewegen.
* diffusie: Gassen kunnen in elkaar diffunderen, wat betekent dat ze spontaan mengen.
Voorbeelden van gassen:
* Zuurstof (O2)
* Stikstof (n2)
* Koolstofdioxide (CO2)
* Helium (hij)
* Methaan (CH4)
Laat het me weten als je nog andere vragen hebt of meer wilt weten over specifieke gassen!
 Zeer efficiënte fotoreductie van kooldioxide, geleid door machine learning en berekening van de eerste principes
Zeer efficiënte fotoreductie van kooldioxide, geleid door machine learning en berekening van de eerste principes  Tweefasig materiaal met verrassende eigenschappen
Tweefasig materiaal met verrassende eigenschappen Wat is het salaris van een scheikundeleraar op een middelbare school?
Wat is het salaris van een scheikundeleraar op een middelbare school?  Welk type binding is propyleenglycol?
Welk type binding is propyleenglycol?  Wat is de normaliteit van geconcentreerd zwavelzuur?
Wat is de normaliteit van geconcentreerd zwavelzuur?
Hoofdlijnen
- Begrijpt jouw hond het als je zegt ‘haal de bal’? Een nieuwe studie in Hongarije zegt van wel
- Fysische principes gebruiken om te begrijpen hoe cellen zichzelf sorteren tijdens hun ontwikkeling
- Een viraal verhulapparaat:Biologen laten zien hoe het menselijke cytomegalovirus zich verbergt voor het immuunsysteem
- Vogelgriep doodt 700 zwarte gieren, sluit dierenasiel
- Mens of zeehond? Wie heeft het beste gehoor onder water?
- Bacteriën coderen voor verborgen genen buiten hun genoom; wij?
- Terwijl de vogelgriep zich verspreidt naar melkkoeien, vertonen de roofvogels uit Minnesota tekenen dat ze een opmerkelijke immuniteit opbouwen
- Een geprioriteerde lijst van invasieve uitheemse soorten die het milieu van het VK bedreigen
- Hoe muizenembryo's links van rechts bepalen
- Zout helpt eiwitten om verder te komen
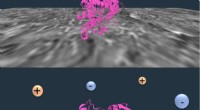
- Hoe bloedcellen vervormen, herstellen wanneer u door kleine kanalen reist
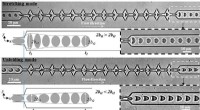
- Wetenschappers ontdekken een betere manier om plastic uit zwavel te maken

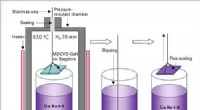
- Ontwikkeling van een nieuwe techniek voor het kweken van hoogwaardige galliumnitridekristallen
- Wetenschappers zetten bier om in brandstof

 Kijk eerst naar zwaartekrachtdans die de vorming van sterren stimuleert
Kijk eerst naar zwaartekrachtdans die de vorming van sterren stimuleert Wat is de volgorde van de planeten van de heetste tot de koudste?
Wat is de volgorde van de planeten van de heetste tot de koudste?  Educatieve interventie verbetert het leren van studenten
Educatieve interventie verbetert het leren van studenten Hoe ecofeminisme werkt
Hoe ecofeminisme werkt  Na 9 maanden in de ruimte, muizensperma levert gezonde muizen op
Na 9 maanden in de ruimte, muizensperma levert gezonde muizen op Welke ionen zijn aanwezig in een oplossing van salpeterzuur?
Welke ionen zijn aanwezig in een oplossing van salpeterzuur?  Het gemiddelde gebied berekenen met behulp van de Neerslagmethode Thiessen
Het gemiddelde gebied berekenen met behulp van de Neerslagmethode Thiessen  Hoe zal het intensiteitsniveau veranderen als de afstand tot een geluidsbron wordt gehalveerd?
Hoe zal het intensiteitsniveau veranderen als de afstand tot een geluidsbron wordt gehalveerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

