
Wetenschap
Hoeveel eenzame paar elektronen rond het centrale atoom in CBR4 is?
Er zijn nul Eenzame paren elektronen rond het centrale koolstofatoom in CBR4.
Dit is waarom:
* koolstof (c) heeft 4 valentie -elektronen.
* bromine (br) heeft 7 valentie -elektronen, maar heeft er slechts 1 nodig om zijn octet te voltooien.
* In CBR4 vormt het koolstofatoom vier enkele bindingen met vier broomatomen. Dit maakt gebruik van alle vier de valentie -elektronen van koolstof.
* Omdat alle valentie -elektronen van koolstof betrokken zijn bij de binding, zijn er geen eenzame paren meer.
Daarom heeft het centrale koolstofatoom in CBR4 geen eenzame paren .
 Een slechte tijd om te leven:studie koppelt deoxygenatie van de oceaan aan oude afsterving
Een slechte tijd om te leven:studie koppelt deoxygenatie van de oceaan aan oude afsterving Portugal worstelt om uit de as van zijn dodelijkste vuur te herrijzen
Portugal worstelt om uit de as van zijn dodelijkste vuur te herrijzen Gebruik van ontdekkingen in de wetenschap om dagelijkse problemen op te lossen?
Gebruik van ontdekkingen in de wetenschap om dagelijkse problemen op te lossen?  De stijgende zeespiegel slokt de stranden van Outer Banks op, nieuw rapport zegt:
De stijgende zeespiegel slokt de stranden van Outer Banks op, nieuw rapport zegt: Wetenschappers oogsten eerste groenten in Antarctische kas
Wetenschappers oogsten eerste groenten in Antarctische kas
Hoofdlijnen
- Hoe wordt eiwitten in een cel gemaakt?
- Waarom is het skeletstelsel belangrijk?
- Wanneer kan het fenotype je genotype van een eigenschap vertellen?
- Zal geautomatiseerde landbouw helpen tegemoet te komen aan de voedselvraag in de wereld?
- Welk proces veroorzaakt een uitwisseling van genetische informatie tussen bacteriële cellen?
- Waarom eten sommige bijenkoninginnen de eieren van hun werkbij?
- Hoe classificeerde Linnaeus organismen op basis van hun overeenkomsten?
- Walvisclans gebruiken vocalisaties om hun cultuur te markeren
- Welke suikers zitten er in RNA?
- Onderzoekers onderzoeken ontstekingsremmende activiteit van curcumine

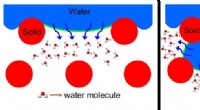
- Wetenschappers onthullen belangrijke inzichten in opkomende waterzuiveringstechnologie
- Antivriesvissen inspireren nieuwe cryoprotectanten voor menselijke cellen en weefsels

- Rekenkracht lost moleculair mysterie op
- Hoeveel pot in die brownie? Chocolade kan tests afwerpen

 Een algemene set principes die worden ondersteund door bewijsmateriaal dat een aspect van de natuur verklaart?
Een algemene set principes die worden ondersteund door bewijsmateriaal dat een aspect van de natuur verklaart?  Een hete en droge Jupiter:SPIRou onthult de atmosfeer van de exoplaneet Tau Boötis b
Een hete en droge Jupiter:SPIRou onthult de atmosfeer van de exoplaneet Tau Boötis b Is er leven op drift in de wolken van Venus?
Is er leven op drift in de wolken van Venus? Nieuwe satelliet wil laten zien hoe AI aardobservatie bevordert
Nieuwe satelliet wil laten zien hoe AI aardobservatie bevordert  Mercurius is een metaal met smeltpunt van -39cc en koken 357cc wat zijn toestand is?
Mercurius is een metaal met smeltpunt van -39cc en koken 357cc wat zijn toestand is?  Hoe kalksteen te schuren
Hoe kalksteen te schuren  Hubble viert zijn 30-jarig jubileum met een tapijt van laaiende stergeboorte
Hubble viert zijn 30-jarig jubileum met een tapijt van laaiende stergeboorte Regelgevende en wetenschappelijke complexiteit van generieke nanodrugs kan besparingen voor patiënten vertragen
Regelgevende en wetenschappelijke complexiteit van generieke nanodrugs kan besparingen voor patiënten vertragen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

