
Wetenschap
Leg uit Hoe vormen de magnesium- en chlooratomen ionen?
1. Elektronenoverdracht:
- Magnesium heeft een lage elektronegativiteit, wat betekent dat het een zwakke aantrekkingskracht heeft op elektronen.
- Chloor heeft een hoge elektronegativiteit, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen.
2. Ionvorming:
- Om een stabielere elektronenconfiguratie te bereiken, heeft magnesium de neiging twee elektronen te verliezen vanaf het buitenste energieniveau (3s²).
- Chloor heeft de neiging één elektron te winnen om zijn buitenste energieniveau (3s²3p⁵) te vullen.
- Als gevolg hiervan verliest magnesium twee elektronen aan chloor, waardoor Mg²⁺-ionen en Cl⁻-ionen worden gevormd.
De algemene ionische vergelijking voor de vorming van magnesiumchloride kan worden weergegeven als:
```
Mg (neutraal) → Mg²⁺ (kation) + 2e⁻
2Cl (neutraal) + 2e⁻ → 2Cl⁻ (anion)
Globaal:Mg + 2Cl → Mg²⁺ + 2Cl⁻
```
De elektrostatische aantrekkingskracht tussen de positief geladen magnesiumionen en de negatief geladen chloride-ionen houdt de ionische verbinding, magnesiumchloride (MgCl₂), samen in een stabiele kristallijne roosterstructuur.
 Wat zijn enkele voorbeelden van zuren, basen en neutrale stoffen?
Wat zijn enkele voorbeelden van zuren, basen en neutrale stoffen?  Wat krijg je als je CH4 in O2 verbrandt?
Wat krijg je als je CH4 in O2 verbrandt?  Rise of the mutants:nieuw onderzoek om enzymontwerpmethodologieën te verbeteren
Rise of the mutants:nieuw onderzoek om enzymontwerpmethodologieën te verbeteren Nieuwe katalysator voor waterstofproductie is een stap in de richting van schone brandstof
Nieuwe katalysator voor waterstofproductie is een stap in de richting van schone brandstof Een nieuwe methode om spiegels van variabele grootte af te drukken met een reflectie van meer dan 99%
Een nieuwe methode om spiegels van variabele grootte af te drukken met een reflectie van meer dan 99%
 Ongrijpbare atmosferische golf gedetecteerd tijdens vulkaanuitbarsting in Tonga
Ongrijpbare atmosferische golf gedetecteerd tijdens vulkaanuitbarsting in Tonga Vulkaan barst uit op Hawaii's Big Island, trekt drukte om te parkeren
Vulkaan barst uit op Hawaii's Big Island, trekt drukte om te parkeren Wat zijn de twee belangrijkste soorten interacties die in milieustudies worden gebruikt?
Wat zijn de twee belangrijkste soorten interacties die in milieustudies worden gebruikt?  Betere bescherming van kritieke pijpleidingen tijdens landbewegingen
Betere bescherming van kritieke pijpleidingen tijdens landbewegingen Kritieke temperatuur voor de levensduur van tropische bomen onthuld
Kritieke temperatuur voor de levensduur van tropische bomen onthuld
Hoofdlijnen
- Onderzoekers ontdekken nieuwe overspraak tussen fytohormonen ethyleen en auxine
- Hoe een filmmaker, een stapel oude schelpen en een stel amateurs de oesterriffen van Australië terugbrengen
- Het benutten van broodvruchtzetmeel voor de productie van bio-ethanol
- Volledige structuur van mitochondriaal respiratoir supercomplex gedecodeerd
- Gele erwten laten veelbelovende resultaten zien als basis voor de kaas van morgen
- Het leven van een albatros:individualiteit aanpakken in populatiestudies
- Hoe insecten verschillende suikers uit elkaar houden
- Wat zijn de twee belangrijkste kenmerken die een wetenschappelijk model moet hebben?
- Onderzoek bevestigt het:we worden echt dommer
- Hoogwaardige katalysatoren met één atoom voor brandstofcellen bij hoge temperaturen

- Chemici ontwikkelen nieuw materiaal voor het scheiden van kooldioxide uit industriële afvalgassen

- Cellulaire stress verdediging
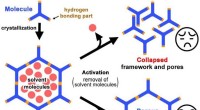
- Poreuze materialen werpen licht op milieuzuivering
- Microscoop voor mobiele telefoons detecteert de stille moordenaar van honingbijen

 NASA vindt windschering die de tropische storm Josephine beïnvloedt
NASA vindt windschering die de tropische storm Josephine beïnvloedt De evolutie van voedingsstrategieën bij oude krokodillen ontrafelen
De evolutie van voedingsstrategieën bij oude krokodillen ontrafelen Studie:genderongelijkheid neemt toe in media tijdens pandemie
Studie:genderongelijkheid neemt toe in media tijdens pandemie De manen van Saturnus:wat een verschil decennium maakt
De manen van Saturnus:wat een verschil decennium maakt  Kun je de kleurvlam voorspellen wanneer chloriden worden verwarmd?
Kun je de kleurvlam voorspellen wanneer chloriden worden verwarmd?  Nieuw kwantumeffect gevonden:Spin-rotatie koppeling
Nieuw kwantumeffect gevonden:Spin-rotatie koppeling Gedraagt zich als een spier, apparaat van nanoformaat tilt 165 keer zijn eigen gewicht op
Gedraagt zich als een spier, apparaat van nanoformaat tilt 165 keer zijn eigen gewicht op Welke invloed heeft vervuiling op bossen?
Welke invloed heeft vervuiling op bossen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

