
Wetenschap
Wat is de bindingssterkte van waterstofbruggen?
Waterstofbindingen zijn geen chemische bindingen, maar eerder niet-covalente interacties tussen een waterstofatoom uit het ene molecuul en een elektronegatief atoom (zoals stikstof, zuurstof of fluor) uit een ander molecuul. De sterkte van waterstofbruggen kan variëren afhankelijk van de elektronegativiteit van de betrokken atomen en de moleculaire omgeving, maar doorgaans varieert deze van 1 tot 40 kJ/mol, aanzienlijk zwakker dan covalente bindingen die doorgaans een bindingssterkte hebben in het bereik van 100 tot 1000 kJ. /mol.
 Bestaat glucose uit koolstofdioxide?
Bestaat glucose uit koolstofdioxide?  Nieuw kristallijn oxide kan het probleem van oververhitting in composietmaterialen oplossen
Nieuw kristallijn oxide kan het probleem van oververhitting in composietmaterialen oplossen Nieuw type glas geïnspireerd door de natuur is beter bestand tegen schokken
Nieuw type glas geïnspireerd door de natuur is beter bestand tegen schokken Onderzoek onthult ontbrekende fysica in explosieve hotspots
Onderzoek onthult ontbrekende fysica in explosieve hotspots Wat is de kleur van methyloranje in alkali?
Wat is de kleur van methyloranje in alkali?
 Antarctische ijskloof verspreidt zich:nieuwe tak onthuld in de nieuwste gegevens van ijsplaat
Antarctische ijskloof verspreidt zich:nieuwe tak onthuld in de nieuwste gegevens van ijsplaat Klimaatonzekerheid verminderen, het verbeteren van de weersvoorspellingen, en inzicht in zeespiegelstijging
Klimaatonzekerheid verminderen, het verbeteren van de weersvoorspellingen, en inzicht in zeespiegelstijging Van droogte tot zondvloed:wat is de toekomst voor Californië?
Van droogte tot zondvloed:wat is de toekomst voor Californië?  Science Activities on Air for Preschool Ages
Science Activities on Air for Preschool Ages Onderzoek toont zes decennia aan verandering in planktongemeenschappen
Onderzoek toont zes decennia aan verandering in planktongemeenschappen
Hoofdlijnen
- Zijn domme mensen gelukkiger?
- Dansgerelateerde wetenschapsprojecten
- Wetenschappers ontdekken hoe sommige bacteriën antibiotica overleven
- Heeft iemand artikelen gepubliceerd met Advances in Microbiology? Ik werd voorgesteld om mijn eigen artikel daarin in te dienen. Wie kan het mij vertellen?
- De Atlantische steuren verblijven
- Nobelprijs:Svante Pääbos oude DNA-ontdekkingen bieden aanwijzingen over wat ons menselijk maakt
- Onderzoekers tonen aan dat grotere plantengemeenschappen productiever zijn en gevoeliger voor klimaatopwarming
- Hoe bacteriën zichzelf verdedigen tegen plasma's
- Wat is BIOENERGetica?
- Detectie van kankermarkers in één molecuul brengt vloeibare biopsie dichter bij de kliniek

- Synergistische katalysatoren voor zeer efficiënte waterstofopslag
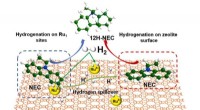
- Nieuw materiaal zou potentieel kunnen ontsluiten voor een revolutie in voertuigen op waterstof
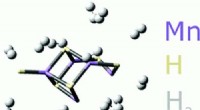
- Membraantechnologie kan emissies en energieverbruik bij olieraffinage verminderen

- Nieuw inzicht in de rijping van miRNA's
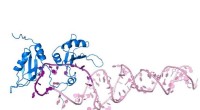
 Landingsplaats Mars 2020 biedt unieke kansen
Landingsplaats Mars 2020 biedt unieke kansen Gletsjers en raadselachtige steenstrepen in de Ethiopische hooglanden
Gletsjers en raadselachtige steenstrepen in de Ethiopische hooglanden Zelfs koude harde contanten zijn niet genoeg stimulans om naar tegengestelde meningen te luisteren
Zelfs koude harde contanten zijn niet genoeg stimulans om naar tegengestelde meningen te luisteren  Onderzoeker kijkt naar de grootste maan van Saturnus
Onderzoeker kijkt naar de grootste maan van Saturnus Newtons converteren naar Mass
Newtons converteren naar Mass Hebben we genoeg om COVID?
Hebben we genoeg om COVID? Hoe een dinosaurus te wegen
Hoe een dinosaurus te wegen  Wat is het kookpunt van water bij -1 bar?
Wat is het kookpunt van water bij -1 bar?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

