
Wetenschap
Hoeveel kooldioxide ontstaat er als 336 g natriumwaterstofcarbonaat volledig afbreekt?
De uitgebalanceerde chemische vergelijking voor de ontleding van natriumwaterstofcarbonaat is:
2NaHCO3(s) → CO2(g) + H2O(g) + Na2CO3(s)
Uit de uitgebalanceerde chemische vergelijking kunnen we zien dat 2 mol NaHCO3 1 mol CO2 produceert.
De molaire massa van NaHCO3 is:
23 g/mol (Na) + 1 g/mol (H) + 12 g/mol (C) + 3(16 g/mol) (O) =84 g/mol
336 g NaHCO3 komt dus overeen met:
336 g / 84 g/mol =4 mol NaHCO3
Volgens de uitgebalanceerde chemische vergelijking zal 4 mol NaHCO3 2 mol CO2 produceren.
De molaire massa van CO2 is:
12 g/mol (C) + 2(16 g/mol) (O) =44 g/mol
Dus 2 mol CO2 weegt:
2 mol * 44 g/mol =88 g CO2
Wanneer 336 g natriumwaterstofcarbonaat volledig wordt afgebroken, produceert het dus 88 g kooldioxide.
 Modellering van lawinebescherming in bossen
Modellering van lawinebescherming in bossen Wat zal er gebeuren met de hydrosfeer en de biosfeer als er geen atmosfeer is?
Wat zal er gebeuren met de hydrosfeer en de biosfeer als er geen atmosfeer is?  Een nadere blik op de creatie van een metamorfe zool
Een nadere blik op de creatie van een metamorfe zool Onderzoekers voeren eerste wereldwijde beoordeling uit van de uitstoot van broeikasgassen in de levenscyclus van kunststoffen
Onderzoekers voeren eerste wereldwijde beoordeling uit van de uitstoot van broeikasgassen in de levenscyclus van kunststoffen Meer eiwitten en goed voor de planeet:9 redenen waarom we microalgen zouden moeten eten
Meer eiwitten en goed voor de planeet:9 redenen waarom we microalgen zouden moeten eten
Hoofdlijnen
- Wat wetenschappers weten over de glans van de juweelkever
- Welke oplossingen vind je in het menselijk lichaam?
- Hoe evolueert het vermijden van inteelt bij planten?
- Van één cel naar vele:hoe is meercelligheid geëvolueerd?
- Onderzoek laat zien hoe genen de bladarchitectuur beïnvloeden
- Het benutten van broodvruchtzetmeel voor de productie van bio-ethanol
- CMU-software assembleert RNA-transcripten nauwkeuriger
- Wat is een celmembraan?
- Onderzoeken hoe gistcellen medicijnen kunnen produceren voor de behandeling van psychotische stoornissen
- Slim bulkplastic reageert op licht, temperatuur en vochtigheid

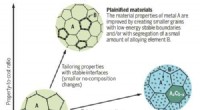
- Verduidelijking belooft veel goeds voor het verbeteren van de duurzaamheid van materialen
- IJzerkatalysator kan belangrijke chemische reacties goedkoper en milieuvriendelijker maken
- Onderzoekers beoordelen de snelle vooruitgang in machine learning voor de chemische wetenschappen

- Onderzoekers ontwikkelen een niet-invasieve test voor rookverontreiniging in wijngaarden

 Onderzoekers verkennen nieuwe diepten in infrarood nanospectroscopie
Onderzoekers verkennen nieuwe diepten in infrarood nanospectroscopie Natuurkundigen gaan op jacht naar een lang gezochte kwantumgloed
Natuurkundigen gaan op jacht naar een lang gezochte kwantumgloed Wat maakt magneten afweren?
Wat maakt magneten afweren?  winden, Overstromingen en brand:record VS voor duur weer
winden, Overstromingen en brand:record VS voor duur weer Satelliet veiliger maken:de zoektocht naar nieuwe drijfgassen
Satelliet veiliger maken:de zoektocht naar nieuwe drijfgassen Beoordeling van de impact van door de mens veroorzaakte uitstoot van stikstof in het milieu
Beoordeling van de impact van door de mens veroorzaakte uitstoot van stikstof in het milieu Waarom zeggen we dat de bodem de basis van het leven is?
Waarom zeggen we dat de bodem de basis van het leven is?  Mechanochemische vorming van peptidebindingen achter de oorsprong van het leven
Mechanochemische vorming van peptidebindingen achter de oorsprong van het leven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

