
Wetenschap
Wat wordt waargenomen als waterige ammoniak in overmaat aan een zilverchloride-oplossing wordt toegevoegd?
1. Aanvankelijk vormt zich een wit neerslag van zilverchloride als gevolg van de reactie tussen zilverionen (Ag+) uit de zilverchloride-oplossing en chloride-ionen (Cl-) uit de waterige ammoniak.
2. Naarmate er meer ammoniak wordt toegevoegd, lost het zilverchlorideneerslag op en vormt een complex ion genaamd diamminezilver(I)-ion ([Ag(NH3)2]+). Dit complexe ion is oplosbaar in water.
3. De oplossing wordt kleurloos naarmate het zilverchlorideneerslag oplost.
De totale reactie kan worden weergegeven als:
AgCl(s) + 2 NH3(aq) -> [Ag(NH3)2]+(aq) + Cl-(aq)
Deze reactie is omkeerbaar en de toevoeging van een overmaat aan ammoniak drijft het evenwicht in de richting van de vorming van het complexe ion.
 Duurzaam, zeer selectieve biokatalytische omzetting van aldehyden in carbonzuren
Duurzaam, zeer selectieve biokatalytische omzetting van aldehyden in carbonzuren Wat zijn de chemische verbindingen in een lippenstift?
Wat zijn de chemische verbindingen in een lippenstift?  Hoe röntgenstralen in de materie genetischtoxische elektronen met lage energie creëren
Hoe röntgenstralen in de materie genetischtoxische elektronen met lage energie creëren  De weg vrijmaken voor kunstmatige fotosynthese:effect van doping op de fotokatalysator SrTiO3
De weg vrijmaken voor kunstmatige fotosynthese:effect van doping op de fotokatalysator SrTiO3 Wat is een overvloedig aanwezig element in zowel watermoleculen als de meeste organische moleculen?
Wat is een overvloedig aanwezig element in zowel watermoleculen als de meeste organische moleculen?
 Onderzoeker onderzoekt hoe het universum rede en moraliteit creëert
Onderzoeker onderzoekt hoe het universum rede en moraliteit creëert  Maakt China zijn klimaatbeloften waar?
Maakt China zijn klimaatbeloften waar? Project werft hulp van burgerwetenschappers om seismische gebeurtenissen te classificeren
Project werft hulp van burgerwetenschappers om seismische gebeurtenissen te classificeren Wereldbevolking zal waarschijnlijk krimpen na het midden van de eeuw, het voorspellen van grote verschuivingen in de wereldbevolking en economische macht
Wereldbevolking zal waarschijnlijk krimpen na het midden van de eeuw, het voorspellen van grote verschuivingen in de wereldbevolking en economische macht Wie zijn de klimaatactivisten van vandaag? Drie grote mythen wegnemen voor Earth Month
Wie zijn de klimaatactivisten van vandaag? Drie grote mythen wegnemen voor Earth Month
Hoofdlijnen
- Hoe IJsland een hoofdrol zou kunnen spelen als duurzame alternatieve eiwitexporteur naar Noord-Europa
- Wat betekent ion?
- Waarom fruit rijpt en bloemen afsterven:Wetenschappers ontdekken hoe belangrijke plantenhormonen worden geactiveerd
- Zullen geavanceerde organismen hetzelfde zijn als complexe organismen, waarom?
- Tsjaad breidt belangrijk natuurgebied in nationaal park uit
- Hoe menselijke cellen de start van DNA-replicatie coördineren
- Welke delen van de cel kun je onder een microscoop* zien?
- Wat zijn de vier belangrijkste methoden voor het produceren van ATP?
- Wat veroorzaakt slaap? Bij fruitvliegjes is het stress op cellulair niveau
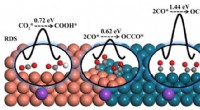
- Afstemming van reactiebarrières voor elektroreductie van kooldioxide tot producten met meerdere koolstofatomen
- Wat zit er in deze plant? Het beste geautomatiseerde systeem voor het vinden van potentiële medicijnen

- Wetenschappers persen katalysatoren in gastheermaterialen zoals een schip in een fles

- DNA-origami overtreft belangrijke drempels

- Structuur van vetverwerkend enzym bepaald
 Hoe houdt evolutie het creationisme in?
Hoe houdt evolutie het creationisme in?  Hoe maak je een Math Brochure
Hoe maak je een Math Brochure  Hoe kan het gebruik van elektriciteit het lichaam genezen?
Hoe kan het gebruik van elektriciteit het lichaam genezen?  Europa plant update op afstand om verouderde Mars-sonde stabiel te houden
Europa plant update op afstand om verouderde Mars-sonde stabiel te houden Eerste onderzoek om te zien of digitale advertenties werken, over millennials
Eerste onderzoek om te zien of digitale advertenties werken, over millennials Hoe maak je een zelfgemaakte onderzeeër voor Science Class
Hoe maak je een zelfgemaakte onderzeeër voor Science Class Hoe het aantal neutronen in een isotoop
Hoe het aantal neutronen in een isotoop Oceanen in overvloed:nieuwe studie suggereert dat de meeste bewoonbare planeten geen droog land hebben
Oceanen in overvloed:nieuwe studie suggereert dat de meeste bewoonbare planeten geen droog land hebben
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

