
Wetenschap
Wat zal de druk doen als het volume en het aantal mol gas constant worden gehouden als de temperatuur stijgt?
Als het volume en het aantal mol van een gas constant worden gehouden, zal het verhogen van de temperatuur ervoor zorgen dat de druk van het gas toeneemt. Deze relatie tussen temperatuur en druk staat bekend als de wet van Charles of de wet van Gay-Lussac.
Volgens de wet van Charles is de druk van een gas recht evenredig met de temperatuur ervan, ervan uitgaande dat het volume en het aantal mol constant blijven. Dit betekent dat naarmate de temperatuur stijgt, de druk van het gas ook toeneemt, en omgekeerd.
Wiskundig gezien kan de wet van Charles worden uitgedrukt als:
P₁/T₁ =P₂/T₂
Waar:
P₁ en P₂ zijn de begin- en einddruk van het gas
T1 en T2 zijn de begin- en eindtemperatuur van het gas
Deze vergelijking laat zien dat de verhouding tussen de druk en de temperatuur van een gas constant blijft als het volume en het aantal mol constant worden gehouden.
 Wetenschappers maken goedkope en veilige elektrokatalysatoren voor brandstofcellen
Wetenschappers maken goedkope en veilige elektrokatalysatoren voor brandstofcellen Synthese van een zeldzaam metaalcomplex van lachgas opent nieuwe perspectieven voor
Synthese van een zeldzaam metaalcomplex van lachgas opent nieuwe perspectieven voor Het creëren van een snellere, on-site manier om bepaalde alkylstoffen te detecteren
Het creëren van een snellere, on-site manier om bepaalde alkylstoffen te detecteren Nuttige verbindingen synthetiseren zonder ongewenste chirale partners te vormen
Nuttige verbindingen synthetiseren zonder ongewenste chirale partners te vormen Hoe goede metalen slecht worden:Discovery verklaart onverwachte eigenschappen van exotische metaalverbindingen
Hoe goede metalen slecht worden:Discovery verklaart onverwachte eigenschappen van exotische metaalverbindingen
Hoofdlijnen
- Afrikaanse gewassen bieden een voedzame, glutenvrije oplossing
- Onderscheid u van de kudde:hoe koeien communiceren gedurende hun leven
- Ontdekt? Nieuw maar uitgestorven menselijk familielid uit Melanesië
- Nieuwe Vincetoxicum-soort gevonden in Yunnan
- Afbraak in het Noordpoolgebied
- Hoe gisten erin slagen de genetische onbalans van extra chromosomen te compenseren
- Uit welke soorten moleculen bestaan RNA-moleculen?
- Negen verdwaalde olifanten geëlektrocuteerd in Botswana
- Wat vormt een peptidebinding?
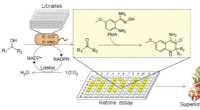
- Nieuwe high-throughput screeningmethode ontwikkeld voor ketonen
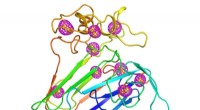
- Nieuwe aanpak voor het oplossen van eiwitstructuren uit minuscule kristallen
- Hout gebruiken in elektroden voor duurzamer, duurzame wearables

- Robuust MOF-materiaal vertoont selectieve, volledig omkeerbare en herhaalbare opvang van giftig atmosferisch gas

- De eerste mechanosynthese van een moleculair kristal met een Borromeaanse topologie

 VRKitchen:een interactieve virtuele omgeving om AI-agenten te trainen en te testen
VRKitchen:een interactieve virtuele omgeving om AI-agenten te trainen en te testen Eight of Swords:de symboliek en interpretatie begrijpen
Eight of Swords:de symboliek en interpretatie begrijpen  Ingenieurs begrijpen nu hoe complexe koolstofnanostructuren ontstaan
Ingenieurs begrijpen nu hoe complexe koolstofnanostructuren ontstaan Neurotransmitters in een oogwenk
Neurotransmitters in een oogwenk Sterke gastheren helpen parasieten zich verder te verspreiden
Sterke gastheren helpen parasieten zich verder te verspreiden Licht als hulpmiddel voor de synthese van complexe moleculen
Licht als hulpmiddel voor de synthese van complexe moleculen Welke vorm van gereduceerd of geoxideerd DCPIP heeft een hogere energiewaarde?
Welke vorm van gereduceerd of geoxideerd DCPIP heeft een hogere energiewaarde?  Hoe positief en negatief geladen ionen zich gedragen op grensvlakken
Hoe positief en negatief geladen ionen zich gedragen op grensvlakken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

