
Wetenschap
Wat verklaart waarom koolstof zo’n veelzijdig element is?
1. Tetravalentie :Koolstofatomen hebben vier valentie-elektronen, wat betekent dat ze vier covalente bindingen kunnen vormen met andere atomen. Hierdoor kan koolstof stabiele, tetraëdrische structuren vormen die de bouwstenen zijn van veel organische moleculen.
2. Catenatie :Koolstofatomen kunnen zich met elkaar binden en zo ketens, ringen en vertakte structuren vormen. Dit vermogen om aan elkaar te binden of met elkaar te verbinden, is wat aanleiding geeft tot de enorme diversiteit aan organische verbindingen.
3. Hybridisatie :Koolstofatomen kunnen hybridisatie ondergaan, wat een proces is waarbij orbitalen worden gemengd om nieuwe atomaire orbitalen te vormen met verschillende vormen en energieën. Hierdoor kan koolstof verschillende soorten bindingen vormen, zoals enkele, dubbele en drievoudige bindingen, en verschillende moleculaire geometrieën aannemen.
4. Functionalisatie :Koolstofatomen kunnen worden gefunctionaliseerd met verschillende functionele groepen, zoals hydroxyl-, carbonyl-, amino- en carboxylgroepen. Deze functionele groepen veranderen de chemische eigenschappen van koolstofatomen en zorgen ervoor dat ze kunnen deelnemen aan een breed scala aan chemische reacties.
5. Hechtsterkte :De covalente bindingen gevormd door koolstofatomen zijn relatief sterk, wat bijdraagt aan de stabiliteit van organische moleculen. Koolstof-koolstofbindingen zijn bijzonder sterk, waardoor op koolstof gebaseerde structuren zeer duurzaam zijn.
6. Elektronegativiteit :Koolstof heeft een intermediaire elektronegativiteit, wat betekent dat het zowel polaire als niet-polaire covalente bindingen kan vormen. Hierdoor kan koolstof interageren met een breed scala aan andere elementen en verbindingen vormen met verschillende polariteiten.
De combinatie van deze factoren maakt koolstof tot een ongelooflijk veelzijdig element dat in staat is een enorme verscheidenheid aan verbindingen te vormen met uiteenlopende structuren en eigenschappen. Deze veelzijdigheid vormt de basis van de organische chemie en is essentieel voor het bestaan en functioneren van levende organismen.
 Hoe een natuurlijke verbinding uit zakpijpen kanker bestrijdt
Hoe een natuurlijke verbinding uit zakpijpen kanker bestrijdt  Hoge druk doet waterstofvarianten instorten
Hoge druk doet waterstofvarianten instorten Een oplossing van natriumcarbonaat Na2CO3 met een molariteit van 0,0100 M bevat equivalenten ionen per liter oplossing?
Een oplossing van natriumcarbonaat Na2CO3 met een molariteit van 0,0100 M bevat equivalenten ionen per liter oplossing?  Hoeveel elektronen zitten er in het koolstofatoom?
Hoeveel elektronen zitten er in het koolstofatoom?  Wat gebeurt er als je een chemische binding laat exploderen?
Wat gebeurt er als je een chemische binding laat exploderen?
 Kan de vergissing in het verwoeste majestueuze Kasjmir-meer worden verholpen?
Kan de vergissing in het verwoeste majestueuze Kasjmir-meer worden verholpen?  Inheemse Groenlandse bevolking is voorstander van winning en export van zand van smeltende ijskap
Inheemse Groenlandse bevolking is voorstander van winning en export van zand van smeltende ijskap 'Zodra studenten hun identiteit kenden, blonken ze uit':hoe praat je over uitmuntendheid in het inheemse onderwijs in Australië
'Zodra studenten hun identiteit kenden, blonken ze uit':hoe praat je over uitmuntendheid in het inheemse onderwijs in Australië  Verzoening van de doelstellingen van het Akkoord van Parijs voor temperatuur, emissies - uit onderzoek blijkt dat twee doelen niet altijd hand in hand gaan
Verzoening van de doelstellingen van het Akkoord van Parijs voor temperatuur, emissies - uit onderzoek blijkt dat twee doelen niet altijd hand in hand gaan Ontbossing wordt aangedreven door wereldwijde markten
Ontbossing wordt aangedreven door wereldwijde markten
Hoofdlijnen
- Antiverouderingsbehandelingen - The Science of Living Longer
- Microbioomtransplantaties bieden ziekteresistentie in ernstig bedreigde Hawaiiaanse plant
- Hoe cellen hun mRNA-voorraad en de output ervan beheren
- Longhornteek voor het eerst ontdekt in het noorden van Missouri
- Waarom alle talen woorden hebben voor 'dit' en 'dat'
- Steur blijft zeldzaam in de Grote Meren, maar de bevolking van Detroit Rivers bloeit
- Wat tanden onthullen over de levens van moderne mensen
- Bacterieel 'schakelgen' reguleert hoe oceanen zwavel in de atmosfeer uitstoten
- Wat doet een luchtpijpcel?
- Een nieuwe eiwit-spin-labelingtechniek
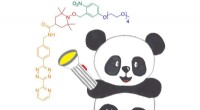
- Nieuwe materialen en processen om pathogene micro-organismen uit water te verwijderen
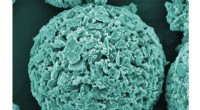
- De efficiëntie van systemen voor het opvangen en omzetten van koolstof verhogen

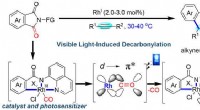
- Zichtbaar licht-geïnduceerde bifunctionele rhodium katalyse ontwikkeld voor decarbonylatieve koppeling van imiden met alkynen
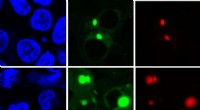
- Nieuwe methode gebruikt fluorescentie om ziekteverwekkende vormen van eiwitten te identificeren
 Waarom wolken het ontbrekende stukje zijn in de puzzel over klimaatverandering
Waarom wolken het ontbrekende stukje zijn in de puzzel over klimaatverandering Wat is het massagetal van een zinkatoom met 37 neutronen?
Wat is het massagetal van een zinkatoom met 37 neutronen?  Quantum computing met gaten
Quantum computing met gaten Laserprinttechnologie produceert binnen enkele minuten waterdicht e-textiel
Laserprinttechnologie produceert binnen enkele minuten waterdicht e-textiel Wat zijn de vier kwadranten in een grafiek?
Wat zijn de vier kwadranten in een grafiek?  Hoeveel lenzen bevinden zich in een samengestelde microscoop?
Hoeveel lenzen bevinden zich in een samengestelde microscoop?  Externe structuur kan de functie van enzymen beïnvloeden
Externe structuur kan de functie van enzymen beïnvloeden AI trainen om een luchtgevecht te winnen
AI trainen om een luchtgevecht te winnen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

