
Wetenschap
Wat is de intermoleculaire binding van methanol?
De intermoleculaire binding van methanol is waterstofbinding. Waterstofbinding is een dipool-dipool-interactie die plaatsvindt tussen een waterstofatoom dat is gebonden aan een zeer elektronegatief atoom (zoals zuurstof, stikstof of fluor) en een ander elektronegatief atoom. In het geval van methanol is het waterstofatoom van de hydroxylgroep gebonden aan het sterk elektronegatieve zuurstofatoom, waardoor een gedeeltelijk positieve lading op het waterstofatoom ontstaat. Deze gedeeltelijk positieve lading kan vervolgens een interactie aangaan met de gedeeltelijk negatieve lading op een ander zuurstofatoom in een nabijgelegen methanolmolecuul, waardoor een waterstofbrug ontstaat.
 HOE 0,1N NaOH-oplossing bereiden?
HOE 0,1N NaOH-oplossing bereiden?  Wetenschappers observeren rechtstreeks de overdracht van licht naar energie in nieuwe zonnecelmaterialen
Wetenschappers observeren rechtstreeks de overdracht van licht naar energie in nieuwe zonnecelmaterialen Hoe flessenwater
Hoe flessenwater  DNA-sjablonen gebruiken om de energie van de zon te benutten
DNA-sjablonen gebruiken om de energie van de zon te benutten Ontwikkeling van een zeer duurzame enkel-atomige katalysator met behulp van industriële luchtbevochtiger
Ontwikkeling van een zeer duurzame enkel-atomige katalysator met behulp van industriële luchtbevochtiger
 Voormalige EPA-adviseurs zeggen dat het kwikvoorstel van bureaus gebrekkig is
Voormalige EPA-adviseurs zeggen dat het kwikvoorstel van bureaus gebrekkig is Verkeersdrempels op Duitse weg om klimaatverandering tegen te gaan
Verkeersdrempels op Duitse weg om klimaatverandering tegen te gaan Hoe protectionisme ontwikkelingslanden kan helpen hun economisch potentieel te ontsluiten
Hoe protectionisme ontwikkelingslanden kan helpen hun economisch potentieel te ontsluiten  Nieuw scenario voor de botsingsdynamiek tussen India en Azië
Nieuw scenario voor de botsingsdynamiek tussen India en Azië Wetenschappers vechten om het regenwoud van DR Congo te beschermen terwijl de bedreigingen toenemen
Wetenschappers vechten om het regenwoud van DR Congo te beschermen terwijl de bedreigingen toenemen
Hoofdlijnen
- Verschillen en overeenkomsten tussen eencellig en cellulair
- Waarom zijn haarvaten slechts één cel dik?
- DNA uit fossiele eierschalen onthult hoe uitgestorven olifantsvogels leefden
- Moet de grijze wolf zijn bedreigde diersoorten beschermen? Nieuw genomisch onderzoek biedt een wetenschappelijk antwoord
- Vroege detectiesysteem voor hinderlijke algenplagende Papahānaumokuākea-riffen
- Wat is de evolutionaire lijn?
- Waarom hebben cellen fosfor nodig?
- Hoe stamcellen werken
- Hoe muizenembryo's links van rechts bepalen
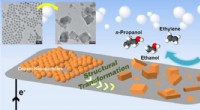
- Koperkatalysator zorgt voor een zeer efficiënte omzetting van CO2 naar brandstoffen
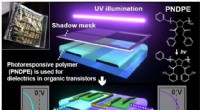
- Flexibele circuits afstemmen met licht
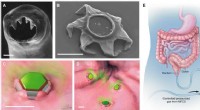
- Gastro-intestinaal-bewoner, vormveranderende microdevices voor verlengde medicijnafgifte
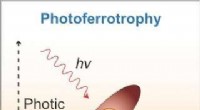
- Deze microben eten elektronen voor energie
- Innovatieve verwerking en verpakking voor veilige, hoge kwaliteit, biologische bessenproducten

 Door stress veroorzaakte embolieën die het watertransport onderbreken, vormen een universeel onderdeel van boomsterfte
Door stress veroorzaakte embolieën die het watertransport onderbreken, vormen een universeel onderdeel van boomsterfte Wat is de betekenis van vervalconstante?
Wat is de betekenis van vervalconstante?  Antarctisch ijskarteringsproject vliegt voor het laatst in oktober
Antarctisch ijskarteringsproject vliegt voor het laatst in oktober Onderzoekers schatten de massa van de Melkweg op 890 miljard keer die van onze zon
Onderzoekers schatten de massa van de Melkweg op 890 miljard keer die van onze zon Hoorzitting Capitol Hill over online haat ziet het uit de eerste hand
Hoorzitting Capitol Hill over online haat ziet het uit de eerste hand Lasers die signalen kunnen verzenden met een snelheid van 224 gigabit per seconde, genoeg om 800 gigabit ethernet te bereiken
Lasers die signalen kunnen verzenden met een snelheid van 224 gigabit per seconde, genoeg om 800 gigabit ethernet te bereiken Kunstmatige intelligentie classificeert supernova-explosies met ongekende nauwkeurigheid
Kunstmatige intelligentie classificeert supernova-explosies met ongekende nauwkeurigheid Virgin Galactic wil binnenkort de ruimte bereiken met toeristische raket
Virgin Galactic wil binnenkort de ruimte bereiken met toeristische raket
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

