
Wetenschap
Ioniseert een zwak zuur bij pH 7?
Zwakke zuren dissociëren gedeeltelijk in water, waarbij H+-ionen en hun geconjugeerde base vrijkomen. De mate van dissociatie wordt bepaald door de zuurdissociatieconstante (Ka) van het zuur. De Ka-waarde geeft de sterkte van het zuur aan; een lagere Ka-waarde betekent dat het zuur zwakker is en minder snel dissocieert.
Bij pH 7 is de concentratie H+-ionen in water 1 x 10^-7 M. Dit betekent dat bij pH 7 het water zelf licht zuur is, met meer H+-ionen dan OH-ionen.
Om een zwak zuur te kunnen ioniseren, moet de concentratie van H+-ionen geproduceerd door de dissociatie van het zuur groter zijn dan 1 x 10^-7 M. Omdat zwakke zuren echter slechts gedeeltelijk dissociëren, is hun bijdrage aan de H+-ionenconcentratie doorgaans verwaarloosbaar. vergeleken met de H+-ionen die al in het water aanwezig zijn bij pH 7.
Daarom ioniseert een zwak zuur niet significant bij pH 7.
 Hoe voorspel je de juiste formule voor een combinatiereactie tussen een niet-metaal en een metaal uit groep A?
Hoe voorspel je de juiste formule voor een combinatiereactie tussen een niet-metaal en een metaal uit groep A?  Wat is het verschil tussen hoge en lage oppervlaktespanning?
Wat is het verschil tussen hoge en lage oppervlaktespanning?  Hoe kun je ionische verbindingen in een zin gebruiken?
Hoe kun je ionische verbindingen in een zin gebruiken?  Wetenschappers berekenen kristalstructuur van superharde molybdeenboriden
Wetenschappers berekenen kristalstructuur van superharde molybdeenboriden Draagbare sensor bewaakt de gezondheid, medicijnen toedient met speeksel en tranen
Draagbare sensor bewaakt de gezondheid, medicijnen toedient met speeksel en tranen
Hoofdlijnen
- Beschrijf hoe de ontwikkeling van de celtheorie aantoont dat wetenschappelijke overtuigingen in de loop van de tijd gebruik kunnen maken van specifieke voorbeelden.
- Hoe boommussen vreemde eieren in hun nesten herkennen
- Percepties van bewoners over de halsbandparkiet in Groot-Brittannië
- Wat is homoloog in de evolutie?
- Theoretisch onderzoek biedt verklaring waarom sommige dieren in de loop van de tijd krimpen
- Kunnen wetenschappers genbewerking gebruiken voor ziektepreventie, maar niet voor menselijke verbetering?
- Hoe een klein deel van de oceanen in de wereld aan de mondiale vraag naar zeevruchten zou kunnen voldoen
- Worden biologische groenten en fruit binnenkort goedkoper?
- Genetische klokken bij zoöplanktonsoorten reguleren wat waarschijnlijk de grootste dagelijkse beweging van biomassa ter wereld is
- Wetenschappers verbeteren kleur en textuur van kweekvlees

- Malaria kaapt je genen om je lever binnen te dringen
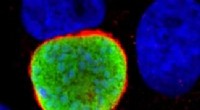
- Lab-on-a-chip helpt bij het zoeken naar menselijk DNA op plaats delict

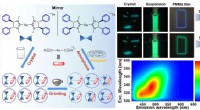
- Wetenschappers stellen nieuwe slimme luminescente materialen van Au(I)-dubbelzouten voor
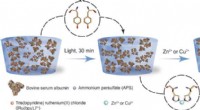
- Kation-geïnduceerde vormprogrammering en morphing in op eiwit gebaseerde hydrogels
 Zorgen over voedselverspilling lijken te verdwijnen wanneer gasten weten dat restjes composteren
Zorgen over voedselverspilling lijken te verdwijnen wanneer gasten weten dat restjes composteren De waarneming van Chern-mozaïek en Berry-curvature-magnetisme in magisch hoekgrafeen
De waarneming van Chern-mozaïek en Berry-curvature-magnetisme in magisch hoekgrafeen Neutronen volgen kwantumverstrengeling in koper-elpasolietmineraal
Neutronen volgen kwantumverstrengeling in koper-elpasolietmineraal The Penguins of the Tundra Biome
The Penguins of the Tundra Biome  Bestaande politieke spanningen nemen toe tijdens pandemie:een glokale observatie
Bestaande politieke spanningen nemen toe tijdens pandemie:een glokale observatie Nieuwe theorie concludeert dat de oorsprong van leven op aardachtige planeten waarschijnlijk is
Nieuwe theorie concludeert dat de oorsprong van leven op aardachtige planeten waarschijnlijk is Hoe een semantische kaart te maken
Hoe een semantische kaart te maken Traditioneel Xuan-papier inspireert ontwikkeling van nieuwe transparante folie met hoge waas
Traditioneel Xuan-papier inspireert ontwikkeling van nieuwe transparante folie met hoge waas
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

