
Wetenschap
Een monster van 7,81 x 10-3 mol zuurstofgas werd in een container van 0,355 liter geplaatst bij 398 K. Wat is de druk kPa die door het gas wordt uitgeoefend?
We kunnen de ideale gasvergelijking gebruiken om de druk van het zuurstofgas te berekenen. De ideale gasvergelijking is:
$$PV =nRT$$
waar:
* P is de druk van het gas in atmosfeer (atm)
* V is het volume van het gas in liters (L)
* n is het aantal mol gas
* R is de ideale gasconstante (0,08206 L atm / mol K)
* T is de temperatuur van het gas in Kelvin (K)
In dit geval hebben we:
* n =7,81x10-3 mol
* V =0,355 L
* T =398 K
Als we deze waarden vervangen door de ideale gasvergelijking, krijgen we:
$$P =\frac{nRT}{V}$$
$$P =\frac{(7,81x10-3 mol)(0,08206 L atm / mol K)(398 K)}{0,355 L}$$
$$P =7,16 atm$$
Atm omrekenen naar kPa:
P =7,16 atm * 101,325 kPa/atm =728 kPa
Daarom is de druk die door het zuurstofgas wordt uitgeoefend 728 kPa.
 In een draai, Colorado vraagt EPA om luchtwaardigheid van staten te verlagen
In een draai, Colorado vraagt EPA om luchtwaardigheid van staten te verlagen Een nieuwe sneeuwstorm treft het noordoosten, dreigt meer uitval
Een nieuwe sneeuwstorm treft het noordoosten, dreigt meer uitval Waar is het vertrouwen? Amerikaanse klimaatontkenners hebben geen vertrouwen in universitaire onderzoekers
Waar is het vertrouwen? Amerikaanse klimaatontkenners hebben geen vertrouwen in universitaire onderzoekers  Wild Squirrels voeden
Wild Squirrels voeden Studie van 14e-eeuwse plaag daagt veronderstellingen over natuurlijke loodniveaus uit
Studie van 14e-eeuwse plaag daagt veronderstellingen over natuurlijke loodniveaus uit
Hoofdlijnen
- Onderzoekers bieden visserij een oplossing voor overbevissing
- Biohazard-afval verwijderen
- Nieuwe atlas biedt ongekende inzichten over hoe genen functioneren in de vroege embryo-ontwikkeling
- Waarom mRNA-blauwdrukken die moeilijker te ontcijferen zijn, een kortere levensduur hebben
- Mensen gebruiken niet zoveel denkkracht als we graag denken
- Wat zijn de twee basismanieren waarop stoffen een cel binnenkomen of verlaten?
- Hoe natuurkunde en biologie samenwerken om de mechanismen van het leven te verkennen
- Wat is de rol van buffers in een cel?
- Onderzoekers ontdekken dat calcium aardappelplanten kan beschermen tegen bacteriële verwelking
- Fruitig met een vleugje schimmel:hoe schimmelinfecties het aroma van wijn veranderen

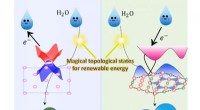
- De waterstofproductie versnellen door de magische topologische oppervlaktetoestanden
- Belangrijke stappen voor het transformeren van giftige moleculen in lucht bij lage temperaturen

- Dominerende schimmel zou een oplossing kunnen zijn om meer biobrandstoffen en chemicaliën te produceren
- Het verminderen van zout in Parmigiano Reggiano-kaas heeft mogelijk geen negatieve invloed op de smaak

 Wat is een hoge latitude?
Wat is een hoge latitude?  Dubbel probleem:overstromingen en COVID-19 zijn samengesmolten en vormen een groot gevaar voor Oost-Timor
Dubbel probleem:overstromingen en COVID-19 zijn samengesmolten en vormen een groot gevaar voor Oost-Timor Target speelt op kracht, digitale verkoop en winkels combineren
Target speelt op kracht, digitale verkoop en winkels combineren CEO Thyssenkrupp treedt af na fusiedeal Tata
CEO Thyssenkrupp treedt af na fusiedeal Tata Hoe snel groeien mannelijke herten geweien?
Hoe snel groeien mannelijke herten geweien?  Geef aan wat er oscilleert in dit type golf?
Geef aan wat er oscilleert in dit type golf?  Geen lancering vanuit Australië - iets ontbreekt in onze plannen voor de nieuwe ruimterace
Geen lancering vanuit Australië - iets ontbreekt in onze plannen voor de nieuwe ruimterace Fotosynthese versus cellulaire ademhaling in elektronenstroom
Fotosynthese versus cellulaire ademhaling in elektronenstroom
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

