
Wetenschap
Wat is de massa van 175 atomen goud?
Om de massa van 175 atomen goud te vinden, moeten we de molaire massa van goud en het getal van Avogadro kennen.
De molaire massa van goud (Au) is 196,97 gram per mol (g/mol). Dit betekent dat één mol goudatomen een massa heeft van 196,97 gram.
Het getal van Avogadro is het aantal deeltjes (atomen, moleculen, ionen, enz.) in één mol van een stof. Het is gelijk aan 6,022 × 10^23 deeltjes per mol.
Nu kunnen we de molaire massa van goud en het getal van Avogadro gebruiken om de massa van 175 goudatomen te vinden:
Aantal atomen goud =175
Massa van 1 atoom goud =196,97 g / 6,022 × 10^23 atomen
Massa van 175 atomen goud =175 × 196,97 g / 6,022 × 10^23 atomen ≈ 5,74 × 10^(-21) gram
Daarom is de massa van 175 goudatomen ongeveer 5,74 × 10^(-21) gram.
 Hoe het periodiek systeem werkt
Hoe het periodiek systeem werkt  Een röntgenfoto maken van een atoombinding
Een röntgenfoto maken van een atoombinding Wat zijn de typische soorten representatieve deeltjes die worden gebruikt in scheikundige berekeningen?
Wat zijn de typische soorten representatieve deeltjes die worden gebruikt in scheikundige berekeningen?  Computationeel onderzoek onthult hoe Ebola-nucleocapside stabiliseert
Computationeel onderzoek onthult hoe Ebola-nucleocapside stabiliseert  Wat zal er hoogstwaarschijnlijk gebeuren met een plant die niet genoeg CO2 ontvangt?
Wat zal er hoogstwaarschijnlijk gebeuren met een plant die niet genoeg CO2 ontvangt?
Hoofdlijnen
- Hoe maak je een Bacterial Flowchart
- Wat is BIOENERGetica?
- Wat is een diatomische reactie?
- Wetenschappers ontdekken hoe hormonen hun effecten bereiken
- Wetenschappers tonen respect voor sommige parasieten
- Hoe zijn de vossenpopulaties in West-Europa in de loop van de tijd veranderd?
- Een vlieg heeft twee allelen voor de kleur van zijn ogen. Het groene allel is recessief en wordt vertegenwoordigd door blauw dominant, p. Als er 28 organismen zijn, welke p?
- Het team uit Hong Kong plant zaden om oude granen te beschermen
- Genetische barcodes worden gebruikt om cruciale populaties in een ecosysteem van koraalriffen te kwantificeren
- Het pad voor cellen verlichten

- Licht schijnend op recombinatiemechanismen in zonnecelmaterialen
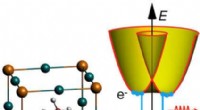
- De code voor roetvorming kraken - wetenschappers ontrafelen mysterie om gevaarlijke emissies te helpen verminderen

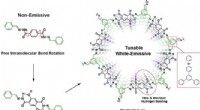
- Afstembaar emissief organisch platform
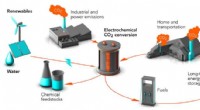
- Kunststoffen, brandstoffen en chemische grondstoffen uit CO2? Ze werken eraan
 Hoe een supernova werkt
Hoe een supernova werkt  De kracht van licht benutten om computers te bedienen
De kracht van licht benutten om computers te bedienen Astronomen identificeren nieuwe asynchrone korte periode polaire
Astronomen identificeren nieuwe asynchrone korte periode polaire Het ecosysteem van Mozambique
Het ecosysteem van Mozambique Toen het lucht- en wegverkeer tijdens COVID daalde, namen ook de luchtvervuilingsniveaus af
Toen het lucht- en wegverkeer tijdens COVID daalde, namen ook de luchtvervuilingsniveaus af Kleine batterij is ook een nanomotor
Kleine batterij is ook een nanomotor Noordoost-VS graaft zich uit van niet-helemaal record sneeuwstorm
Noordoost-VS graaft zich uit van niet-helemaal record sneeuwstorm De regels voor het verdelen van exponenten
De regels voor het verdelen van exponenten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

