
Wetenschap
Welke moleculen bevatten een niet-polaire covalente binding?
Hier zijn enkele aanvullende voorbeelden van moleculen die niet-polaire covalente bindingen bevatten:
* Ethaan (C2H6)
* Propaan (C3H8)
* Butaan (C4H10)
* Pentaan (C5H12)
* Hexaan (C6H14)
* Octaan (C8H18)
* Decaan (C10H22)
* Cyclohexaan (C6H12)
* Benzeen (C6H6)
* Ethyleen (C2H4)
* Propeen (C3H6)
* Buteen (C4H8)
* Penteen (C5H10)
* Hexeen (C6H12)
* Octeen (C8H16)
* Decene (C10H20)
Dit zijn slechts enkele voorbeelden van de vele moleculen die niet-polaire covalente bindingen bevatten. Niet-polaire covalente bindingen zijn het meest voorkomende type chemische binding en worden aangetroffen in een grote verscheidenheid aan stoffen, waaronder gassen, vloeistoffen en vaste stoffen.
 Het maken van middeleeuwse bling
Het maken van middeleeuwse bling Onderzoekers ontwikkelen 3D-geprinte biomaterialen die op verzoek worden afgebroken
Onderzoekers ontwikkelen 3D-geprinte biomaterialen die op verzoek worden afgebroken Wanneer ionische bindingen verbindingen vormen, heeft elk atoom een stabiel octet en wat is elektrisch?
Wanneer ionische bindingen verbindingen vormen, heeft elk atoom een stabiel octet en wat is elektrisch?  Mogelijke nieuwe antivirale middelen tegen COVID-19, herpes
Mogelijke nieuwe antivirale middelen tegen COVID-19, herpes De zon vangen:nieuwe dunnefilmtechnologie maakt gebruik van duurzame componenten voor zonnepanelen
De zon vangen:nieuwe dunnefilmtechnologie maakt gebruik van duurzame componenten voor zonnepanelen
 Kan een tropische watervlo Europese meren binnendringen?
Kan een tropische watervlo Europese meren binnendringen?  Hoe het eerste katachtige sabeltandroofdier werd ontdekt en waarom het verschilt van moderne katten
Hoe het eerste katachtige sabeltandroofdier werd ontdekt en waarom het verschilt van moderne katten  Nepalese klimmers overwonnen verraderlijke omstandigheden om geschiedenis te schrijven op K2
Nepalese klimmers overwonnen verraderlijke omstandigheden om geschiedenis te schrijven op K2 Lichtvervuiling:de donkere kant van het aanhouden van de lichten
Lichtvervuiling:de donkere kant van het aanhouden van de lichten Een laatste paper van wetenschappers kijkt naar het toekomstige klimaat van de aarde
Een laatste paper van wetenschappers kijkt naar het toekomstige klimaat van de aarde
Hoofdlijnen
- Onderzoekers bestuderen de complexiteit van homologe recombinatie en abnormale chromosoombruggen
- Uit onderzoek blijkt dat wilde en gedomesticeerde hoefdieren de sleutel zijn tot de duurzaamheid van het mediterrane ecosysteem
- Trekken STEM-velden meer jongens of meisjes aan? Een nieuwe studie werpt licht
- Proteomics-onderzoek levert aanwijzingen op over de manier waarop tuberculose het immuunsysteem zou kunnen dwarsbomen
- Het doden van slechts een paar dieren zal geen kwaad doen, of toch wel?
- Hoe een Antarctische worm antivries maakt en wat dat met klimaatverandering te maken heeft
- Hoe cellulaire vingertoppen cellen kunnen helpen met elkaar te ‘praten’
- Van druppel tot ontdekking
- Waarom is een atom elektrisch neutraal?
- Onderzoekers ontwikkelen nieuwe elektrodestructuur voor secundaire batterij in vaste toestand

- CryoEM-onderzoek legt opioïde-signalering vast
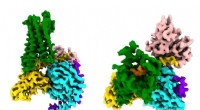
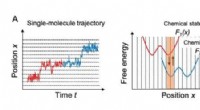
- Nieuwe methode detecteert snel sporen van kleine moleculen
- Het veelzijdige ontwerp van de bidsprinkhaangarnalenclub inspireert geavanceerde composietmaterialen voor vliegtuigen, voetbal helmen
- Wiskundige modellering laat zien hoe chitinase, een moleculaire monorail, gehoorzaamt aan eenrichtingsverkeer
 NASA vindt ex-tropische cycloon Esther terug landinwaarts
NASA vindt ex-tropische cycloon Esther terug landinwaarts Hoe jonge vogels en hun ouders onderhandelen over de beste tijd voor jonge vogels om het nest te verlaten
Hoe jonge vogels en hun ouders onderhandelen over de beste tijd voor jonge vogels om het nest te verlaten  Menselijk afval omzetten in plastic, voedingsstoffen kunnen helpen bij ruimtereizen over lange afstanden
Menselijk afval omzetten in plastic, voedingsstoffen kunnen helpen bij ruimtereizen over lange afstanden Nieuwe perspectieven op hoe ecologische gemeenschappen worden samengesteld
Nieuwe perspectieven op hoe ecologische gemeenschappen worden samengesteld  10 jaar later:hoe door Syrische vluchtelingen geleide bevoorradingsnetwerken de levenskwaliteit verbeteren
10 jaar later:hoe door Syrische vluchtelingen geleide bevoorradingsnetwerken de levenskwaliteit verbeteren  Belangrijke mijlpaal voor kernfusie bereikt toen ontsteking in een laboratorium werd geactiveerd
Belangrijke mijlpaal voor kernfusie bereikt toen ontsteking in een laboratorium werd geactiveerd Elektrisch geladen stofstormen stimuleren de chloorcyclus van Mars
Elektrisch geladen stofstormen stimuleren de chloorcyclus van Mars Onderzoek toont aan dat extracellulaire blaasjes ook berichten van niet-menselijke cellen kunnen overbrengen
Onderzoek toont aan dat extracellulaire blaasjes ook berichten van niet-menselijke cellen kunnen overbrengen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

