
Wetenschap
Wat is waar over de eigenschappen van elementen in een periodiek periodiek systeem?
1. Atoomnummer :Het atoomnummer van elementen neemt gedurende de periode van links naar rechts toe. Dit betekent dat het aantal protonen in de kern van het ene element naar het volgende toeneemt.
2. Metaalachtig karakter :Het metaalachtige karakter neemt in de loop van de periode van links naar rechts af. Dit betekent dat elementen aan de linkerkant van de periode doorgaans reactievere metalen zijn, terwijl die aan de rechterkant minder reactieve niet-metalen zijn.
3. Niet-metalen karakter :Omgekeerd neemt het niet-metalen karakter in de loop van de periode van links naar rechts toe. Elementen aan de rechterkant van de periode vormen waarschijnlijker covalente verbindingen, terwijl die aan de linkerkant de neiging hebben ionische verbindingen te vormen.
4. Atoomstraal :De atoomstraal neemt over het algemeen af van links naar rechts over de periode. Naarmate het atoomnummer toeneemt, worden er meer protonen aan de kern toegevoegd, waardoor de positieve lading toeneemt en de elektronen dichter bij de kern worden getrokken, waardoor de atoomstraal kleiner wordt.
5. Ionisatie-energie :De ionisatie-energie neemt in de loop van de periode doorgaans van links naar rechts toe. Het wordt steeds moeilijker om een elektron uit een atoom te verwijderen naarmate het aantal protonen in de kern toeneemt.
6. Elektronenaffiniteit :Elektronenaffiniteit, de energieverandering die optreedt wanneer een atoom een elektron accepteert, vertoont over het algemeen een onregelmatige trend over een bepaalde periode.
7. Elektronegativiteit :Elektronegativiteit, het vermogen van een atoom om elektronen aan te trekken, neemt in de loop van de periode doorgaans van links naar rechts toe. Dit komt door de toegenomen effectieve nucleaire lading die elektronen ervaren naarmate het atoomnummer toeneemt.
 Bacteriën die giftige metalen binden:zijn zij de toekomst van het opruimen van kernafval?
Bacteriën die giftige metalen binden:zijn zij de toekomst van het opruimen van kernafval?  Metalen stimuleren een veelbelovende methode om schadelijke kooldioxide onder de zee te begraven
Metalen stimuleren een veelbelovende methode om schadelijke kooldioxide onder de zee te begraven Platform met hoge doorvoer maakt het in kaart brengen van activiteiten van opkomende kankergeneesmiddelen mogelijk
Platform met hoge doorvoer maakt het in kaart brengen van activiteiten van opkomende kankergeneesmiddelen mogelijk Onderzoek suggereert dat helium een oppasrol speelt bij het vormen van stabiele chemische verbindingen onder hoge druk
Onderzoek suggereert dat helium een oppasrol speelt bij het vormen van stabiele chemische verbindingen onder hoge druk Niet-giftige technologie haalt meer goud uit erts
Niet-giftige technologie haalt meer goud uit erts
 Waarom wetenschappers zich zorgen maken over de effecten van niet-inheemse paarden en ezels op natuurlijke ecosystemen
Waarom wetenschappers zich zorgen maken over de effecten van niet-inheemse paarden en ezels op natuurlijke ecosystemen  Energiestroom en chemische cyclus door Ecosystem
Energiestroom en chemische cyclus door Ecosystem Zoutconcentraties in ijskernen kunnen recept voor DO-evenementen onthullen
Zoutconcentraties in ijskernen kunnen recept voor DO-evenementen onthullen Versnipperde bossen:Boombedekking, stedelijke wildgroei is de afgelopen 30 jaar beide toegenomen in Zuidoost-Michigan
Versnipperde bossen:Boombedekking, stedelijke wildgroei is de afgelopen 30 jaar beide toegenomen in Zuidoost-Michigan Soldaten ingezet om bosbranden in Engeland te bestrijden
Soldaten ingezet om bosbranden in Engeland te bestrijden
Hoofdlijnen
- Elektronenmicroscopie laat zien hoe vitamine A de cel binnenkomt
- Gene ontdekking kan cassaveziekte bestrijden, voedselzekerheid vergroten
- Neurale opnames van wilde vleermuizen onthullen een unieke organisatie van het middenhersenengebied voor het volgen en vangen van prooien
- DNA-modellen van paperclips maken
- Welk proces produceert klonen?
- Het genoom van de zeekomkommer wijst op genen voor weefselregeneratie
- Hoe kan een fout tijdens de transcriptie het geproduceerde eiwit beïnvloeden?
- Wat zijn de functies van Triglyceride Phospholipid & Sterol?
- Tand snel, tand nieuwsgierig? Nieuwe studie onthult een nieuwe benadering van plantaardig dieet en unieke dinosaurussen met lange nek
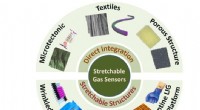
- Onderzoekers ontwikkelen sensoren die menselijke biomarkers en giftig gas detecteren
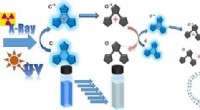
- Onzichtbare röntgenstralen worden blauw
- Belastingregel voor industrie beloont afvang van koolstof

- Moleculaire modelleringskit ter grootte van een micrometer toont echte chemische reacties

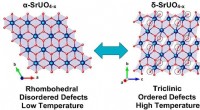
- Uranium gebruiken om orde te scheppen in wanorde
 Nieuwe methode versnelt 3D-printen van millimeterformaat imaging-lenzen
Nieuwe methode versnelt 3D-printen van millimeterformaat imaging-lenzen Onderzoekers rapporteren nieuwe oxyfluorideverbinding voor fotokatalyse
Onderzoekers rapporteren nieuwe oxyfluorideverbinding voor fotokatalyse Onderzoekers gebruiken mysterieuze Casimir-kracht voor kleine apparaten
Onderzoekers gebruiken mysterieuze Casimir-kracht voor kleine apparaten Napoleontische juwelen schitteren op veiling in Genève
Napoleontische juwelen schitteren op veiling in Genève Met nanodeeltjes versierde cellen zorgen voor een nieuwe benadering van kankertherapie
Met nanodeeltjes versierde cellen zorgen voor een nieuwe benadering van kankertherapie Geen pauze in de opwarming van de aarde in de afgelopen 100 jaar
Geen pauze in de opwarming van de aarde in de afgelopen 100 jaar Waarom kunnen bepaalde Bugs op het water lopen?
Waarom kunnen bepaalde Bugs op het water lopen?  Vulkaanuitbarsting waargenomen door prehistorische mensen
Vulkaanuitbarsting waargenomen door prehistorische mensen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

