
Wetenschap
Waarom vervang je 3MH2SO4 door HNO3?
Beschikbaarheid en kosten :3M H2SO4 is over het algemeen gemakkelijker verkrijgbaar en goedkoper in vergelijking met HNO3.
Veiligheidsoverwegingen :Geconcentreerd HNO3 is een sterk oxiderend zuur en kan gevaarlijk zijn bij het hanteren ervan. Het produceert giftige dampen en is bijtend voor de huid en de luchtwegen. 3M H2SO4 daarentegen is minder corrosief en geeft geen schadelijke dampen af. Dit maakt het veiliger om te hanteren en te transporteren.
Compatibiliteit :3M H2SO4 is compatibel met een breder scala aan materialen, waaronder metalen en kunststoffen, vergeleken met HNO3. Dit maakt hem geschikt voor gebruik in verschillende toepassingen en omgevingen.
Zuursterkte :Zowel 3M H2SO4 als HNO3 zijn sterke zuren, maar H2SO4 wordt als een sterker zuur beschouwd dan HNO3. Dit betekent dat 3M H2SO4 effectiever kan zijn bij bepaalde reacties of processen waarbij een sterker zuur vereist is.
Stabiliteit :3M H2SO4 is stabieler en ondergaat niet zo gemakkelijk ontleding of reageert met luchtvochtigheid als HNO3. Dit maakt het een betrouwbaarder en consistenter reagens voor langdurige opslag en gebruik.
Het is echter belangrijk op te merken dat 3M H2SO4 mogelijk niet in alle situaties een directe vervanging voor HNO3 is. De specifieke toepassing, het gewenste resultaat en de compatibiliteitsfactoren moeten zorgvuldig in overweging worden genomen bij het kiezen van het juiste zuur voor een bepaald doel. Bij twijfel is het altijd raadzaam om deskundigen of technische literatuur te raadplegen om een veilig en effectief gebruik van deze zuren te garanderen.
 Endotherme ladingsoverdracht bemiddelt ondiepe afstandsafhankelijke triplet-energiemigratie
Endotherme ladingsoverdracht bemiddelt ondiepe afstandsafhankelijke triplet-energiemigratie Hoe H2S-granen worden geconverteerd naar onderdelen per miljoen
Hoe H2S-granen worden geconverteerd naar onderdelen per miljoen  Wat is een covalente netwerkbinding?
Wat is een covalente netwerkbinding?  Hoe ontvouwen cellulaire machines verkeerd gevouwen eiwitten?
Hoe ontvouwen cellulaire machines verkeerd gevouwen eiwitten? Ontwikkeling van aanpasbare biokleefstoffen voor gepersonaliseerde medische reparaties
Ontwikkeling van aanpasbare biokleefstoffen voor gepersonaliseerde medische reparaties
 Enorme bosbrand bij Lake Tahoe vertraagt naarmate het weer verbetert
Enorme bosbrand bij Lake Tahoe vertraagt naarmate het weer verbetert Model voorspelt stedelijke ontwikkeling en broeikasgassen zullen stedelijke overstromingen aanwakkeren
Model voorspelt stedelijke ontwikkeling en broeikasgassen zullen stedelijke overstromingen aanwakkeren Deadlines kunnen effectief zijn bij het opbouwen van steun voor maatregelen tegen klimaatverandering
Deadlines kunnen effectief zijn bij het opbouwen van steun voor maatregelen tegen klimaatverandering Wetenschappers stellen voor dat vibrios een belangrijke rol spelen in de mariene organische koolstofcyclus
Wetenschappers stellen voor dat vibrios een belangrijke rol spelen in de mariene organische koolstofcyclus Onderzoeker ontdekt hoe je vrouwelijke interesse in wetenschapsstudie kunt aanwakkeren en behouden
Onderzoeker ontdekt hoe je vrouwelijke interesse in wetenschapsstudie kunt aanwakkeren en behouden
Hoofdlijnen
- Hoe oud is mijn huisdier in honden- of kattenjaren? Een dierenarts legt het uit
- Waarom houden we van bijen, maar haten we wespen?
- Onderzoek onthult hoe twee geslachtschromosomen communiceren tijdens de ontwikkeling van vrouwelijke embryo's
- Hebben slakken hun slijmsporen nodig om vooruit te komen? Het is een lastige vraag
- Genetica van waardplanten bepaalt welke micro-organismen ze aantrekken, zo blijkt uit onderzoek
- Onderzoekers ontdekken wat vampierinktvissen eten:dat denk jij niet (Update)
- Hoe de landbouw zou kunnen veranderen in een wereld na de groei
- Onderzoekers beschrijven hoe cellen het afval buiten zetten om ziekten te voorkomen
- Experimenten tonen aan dat de gegevens over het vroege leven volledig 'vals-positieven' kunnen zijn
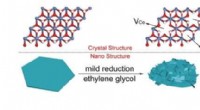
- Rijke defecten die de zuurstofontwikkelingsreactie stimuleren
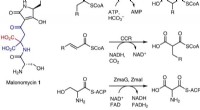
- Wetenschappers ontdekken nieuwe route naar antibiotica met behulp van genbewerking
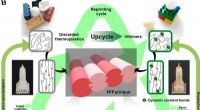
- Upcycling van kunststoffen door dynamische cross-linking
- Ozon breekt THC af dat is afgezet op oppervlakken van derdehands cannabisrook

- Eenvoudige methode om koolstofdioxide om te zetten in bruikbare verbindingen

 Wetenschappers ontwikkelen hardware op atomaire schaal om natuurlijke computers te implementeren
Wetenschappers ontwikkelen hardware op atomaire schaal om natuurlijke computers te implementeren Baanbrekende studie van celsignalering belooft veel voor immuunonderzoek en daarbuiten
Baanbrekende studie van celsignalering belooft veel voor immuunonderzoek en daarbuiten Superoxide produceert hydroxylradicalen die opgeloste organische stoffen in water afbreken
Superoxide produceert hydroxylradicalen die opgeloste organische stoffen in water afbreken Asteroïde Ryugu-stof afgeleverd aan de aarde; Astrobiologen van NASA bereiden zich voor om het te onderzoeken
Asteroïde Ryugu-stof afgeleverd aan de aarde; Astrobiologen van NASA bereiden zich voor om het te onderzoeken UWE bestudeert reistijd - is het echt verspild?
UWE bestudeert reistijd - is het echt verspild?  Maakt naming and shaming van hogescholen met grote collegegeldverhogingen een verschil?
Maakt naming and shaming van hogescholen met grote collegegeldverhogingen een verschil? Google HR-chef stapt opzij naarmate werknemersactivisme toeneemt
Google HR-chef stapt opzij naarmate werknemersactivisme toeneemt Orale medicijnen ontwikkelen die efficiënter werken
Orale medicijnen ontwikkelen die efficiënter werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

