
Wetenschap
Waarom is diamant zo’n harde en niet-reactieve stof?
1. Covalente binding:
- Diamanten zijn volledig samengesteld uit koolstofatomen die zijn gerangschikt in een zeer stijve en dicht opeengepakte kristallijne structuur die bekend staat als een diamanten kubieke structuur.
- Elk koolstofatoom in een diamant vormt covalente bindingen met de vier aangrenzende koolstofatomen, waardoor een zeer stabiele elektronenconfiguratie ontstaat.
- Covalente bindingen omvatten het delen van elektronen tussen atomen, wat resulteert in een sterke interatomaire kracht die de koolstofatomen stevig bij elkaar houdt.
2. Tetraëdrische bindingsregeling:
- In de kubusvormige diamantstructuur bevindt elk koolstofatoom zich in het midden van een tetraëder, omgeven door vier andere koolstofatomen op de hoeken.
- Deze tetraëdrische opstelling resulteert in een symmetrische en uniforme verdeling van elektronen, wat leidt tot uitzonderlijke sterkte en stabiliteit.
3. Sterke koolstof-koolstofbindingen:
- De covalente bindingen tussen koolstofatomen in een diamant zijn ongelooflijk sterk, met een bindingsenergie van 348 kilojoule per mol.
- Deze hoge bindingsenergie komt voort uit de hoge elektronegativiteit van koolstof, waardoor de elektronen gelijkmatig over de atomen worden verdeeld, waardoor een sterke aantrekkingskracht ontstaat en een lage neiging om met andere elementen te reageren.
4. Gebrek aan gebreken:
- De zuiverheid van een diamant speelt een cruciale rol in zijn hardheid en niet-reactiviteit.
- Diamanten met minder defecten, zoals vacatures, onzuiverheden of dislocaties, hebben een robuustere en uniformere kristalstructuur, waardoor ze beter bestand zijn tegen vervorming en chemische reacties.
5. Hoge thermische geleidbaarheid:
- Diamanten hebben een uitzonderlijk hoge thermische geleidbaarheid, waardoor ze warmte efficiënt kunnen afvoeren.
- De sterke covalente bindingen in diamanten vergemakkelijken de snelle overdracht van warmte door het kristalrooster, waardoor plaatselijke verhitting wordt voorkomen en de structuur van de diamant wordt beschermd.
Als gevolg van deze unieke structurele kenmerken en sterke covalente binding bezitten diamanten een opmerkelijke hardheid, waardoor ze het hardste natuurlijke materiaal zijn dat op aarde bekend is. Ze zijn ook bestand tegen chemische reacties en transformaties, waardoor ze in de meeste omgevingen zeer niet-reactief en niet-reactief zijn.
 Filippijns toeristisch eiland worstelt terwijl sluiting opdoemt
Filippijns toeristisch eiland worstelt terwijl sluiting opdoemt Hoe werkte de geest van onze voorouders werkelijk?
Hoe werkte de geest van onze voorouders werkelijk?  'Ondernemersgeest':een product van nature of nurture?
'Ondernemersgeest':een product van nature of nurture?  Microplastics in drinkwater voorlopig geen gezondheidsrisico:WHO
Microplastics in drinkwater voorlopig geen gezondheidsrisico:WHO De kunst van het overtuigen:zijn consumenten geïnteresseerd in abstracte of concrete kenmerken?
De kunst van het overtuigen:zijn consumenten geïnteresseerd in abstracte of concrete kenmerken?
Hoofdlijnen
- Hoe beïnvloedt DNA-replicatie je lichaam?
- Hoe verhindert de afwezigheid van een nucleaire envelop in prokaryoten de controle van genexpressie door RNA na transcriptie te modificeren?
- Hoe een moleculair signaal plantencellen helpt beslissen wanneer ze olie moeten maken
- Stadia van een typische celcyclus
- Team onderzoekt hoe egoïstische genen mannelijke onvruchtbaarheid veroorzaken bij bloeiende planten
- Hier reisden de wolven uit Colorado in mei, ook dichter bij enkele I-70 berggemeenschappen
- Onderzoek naar schapengenen kan helpen om gezondere dieren te fokken
- Hoe Staphylococcus tussen biologische omgevingen glijdt
- Welk enzym voegt nucleïnezuren toe aan de DNA-keten?
- Recycling geeft nieuwe bestemming aan verbruikte splijtstof

- Een snelwegtunnel maken voor ionen

- Biochemici ontdekken mechanisme dat griepvirussen helpt evolueren

- Nieuwe techniek maakt ruimtelijke scheiding van peptidestructuren mogelijk

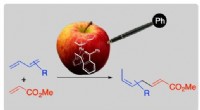
- Fenyltoevoeging maakte een gif bruikbaar voor een chemische reactie bij katalyse
 Hoe een TI-30XA te gebruiken
Hoe een TI-30XA te gebruiken  Studie van vroegere Zuid-Aziatische moessons suggereert sterkere moessonregens in de toekomst
Studie van vroegere Zuid-Aziatische moessons suggereert sterkere moessonregens in de toekomst De grafeen-stamboom definiëren
De grafeen-stamboom definiëren Zonnemateriaal kan onvolkomenheden zelf herstellen, nieuw onderzoek toont aan
Zonnemateriaal kan onvolkomenheden zelf herstellen, nieuw onderzoek toont aan Waarom migreren vogels?
Waarom migreren vogels?  Zeebodem van Fram Strait is een gootsteen voor microplastic uit de Arctische en Noord-Atlantische Oceaan
Zeebodem van Fram Strait is een gootsteen voor microplastic uit de Arctische en Noord-Atlantische Oceaan Recente ontwikkelingen bij de toepassing van polysachariden in cosmetica
Recente ontwikkelingen bij de toepassing van polysachariden in cosmetica  Zo maak je volgens scheikundigen de perfecte pavlova
Zo maak je volgens scheikundigen de perfecte pavlova
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

