
Wetenschap
Leg uit hoe de rangschikking van elektronen in een atoom verband houdt met het periodiek systeem?
1. Atoomnummer: Aan elk element in het periodiek systeem wordt een atoomnummer toegewezen, dat het aantal protonen in zijn kern vertegenwoordigt. In een neutraal atoom is het aantal elektronen gelijk aan het atoomnummer. Het periodiek systeem is horizontaal gerangschikt door het atoomnummer te verhogen.
2. Elektronenschillen: Elektronen in een atoom zijn georganiseerd in schillen of energieniveaus op basis van hun afstand tot de kern. Elke schil kan een bepaald maximaal aantal elektronen bevatten. Schelpen worden aangeduid met K, L, M, N, enzovoort, terwijl ze zich van de kern af bewegen.
3. Periodieke trends: De rangschikking van elektronen in schillen helpt de periodieke trends in de eigenschappen van elementen te verklaren. Elementen in dezelfde groep (verticale kolom) van het periodiek systeem hebben bijvoorbeeld vergelijkbare chemische eigenschappen omdat ze hetzelfde aantal valentie-elektronen hebben:de elektronen in de buitenste schil.
4. Valentie-elektronen: Valentie-elektronen bepalen de chemische reactiviteit van een element en spelen een cruciale rol bij het vormen van bindingen met andere atomen. Elementen in dezelfde periode (horizontale rij) van het periodiek systeem hebben hetzelfde aantal elektronenschillen, maar verschillen in het aantal valentie-elektronen. Deze variatie geeft aanleiding tot verschillen in hun chemisch gedrag.
5. Elektronenconfiguratie: De elektronenconfiguratie van een atoom beschrijft de rangschikking van zijn elektronen in orbitalen binnen elke schil. Elementen met vergelijkbare elektronenconfiguraties hebben de neiging chemische eigenschappen te delen, wat leidt tot periodieke trends in het periodiek systeem.
6. Groeps- en periodeclassificatie: Het periodiek systeem is verdeeld in groepen (verticale kolommen) en perioden (horizontale rijen). Elementen in dezelfde groep delen vergelijkbare chemische eigenschappen omdat ze hetzelfde aantal valentie-elektronen hebben. Elementen in dezelfde periode hebben hetzelfde aantal elektronenschillen.
Over het geheel genomen weerspiegelt het periodiek systeem het toenemende atoomnummer en de systematische rangschikking van elektronen in atomen. Door de elektronenconfiguraties en valentie-elektronen van elementen te begrijpen, kunnen scheikundigen hun chemisch gedrag voorspellen en de periodiciteit verklaren die in hun eigenschappen wordt waargenomen. Deze organisatie biedt een waardevol hulpmiddel voor het bestuderen en voorspellen van het gedrag van elementen, waardoor hun efficiënte classificatie en begrip op het gebied van de chemie wordt vergemakkelijkt.
 Wat is een overgangselement uit periode 4 dat 3 diamagnetische ionen vormt?
Wat is een overgangselement uit periode 4 dat 3 diamagnetische ionen vormt?  Fysische modellen definiëren beter wat pasta ‘al dente’ maakt
Fysische modellen definiëren beter wat pasta ‘al dente’ maakt  Machine learning stimuleert de zoektocht naar superharde materialen
Machine learning stimuleert de zoektocht naar superharde materialen Op licht gebaseerde productie van moleculen voor het ontdekken van geneesmiddelen
Op licht gebaseerde productie van moleculen voor het ontdekken van geneesmiddelen Een slim isotopenscheidingssysteem ontwikkelen
Een slim isotopenscheidingssysteem ontwikkelen
 Tropische storm Jongdari maakt zich op om tyfoon te worden
Tropische storm Jongdari maakt zich op om tyfoon te worden Gedigitaliseerde gegevens van natuurcentra laten de meest voorkomende manieren zien waarop mensen wilde dieren schade toebrengen
Gedigitaliseerde gegevens van natuurcentra laten de meest voorkomende manieren zien waarop mensen wilde dieren schade toebrengen  Darwin 2.0:Wetenschappers werpen nieuw licht op hoe soorten uiteenlopen
Darwin 2.0:Wetenschappers werpen nieuw licht op hoe soorten uiteenlopen  Een nachtzicht van NASA-NOAA vindt een iets beter georganiseerde tropische storm Karina
Een nachtzicht van NASA-NOAA vindt een iets beter georganiseerde tropische storm Karina Feiten over Zebra Babies
Feiten over Zebra Babies
Hoofdlijnen
- Verdeel en definieer:aanwijzingen om te begrijpen hoe stamcellen verschillende soorten produceren
- Wat is een methode om kopieën van DNA te maken?
- Wat is de relatie tussen het ademhalingsproces en de cellulaire ademhaling?
- Kan lachen ziekten genezen?
- Nieuw model voor het analyseren van kleurwaarneming bij bladluizen
- Heeft de gezondheidsstatus van de vader bij muggen invloed op de resultaten van de nakomelingen van de moeder?
- Kunnen mechanismen die tijdens de winterslaap worden gebruikt, dieren helpen nieuwe habitats te koloniseren?
- Waarom het idee dat het Engels een gemeenschappelijke Angelsaksische oorsprong heeft, een mythe is
- De illegale schildpaddenhandel - waarom wetenschappers geheimen bewaren
- Diepeutectische oplosmiddelen vervangen vervuilende industriële oplosmiddelen

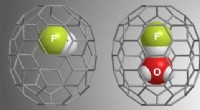
- Onderzoekers isoleren waterstoffluoride en water om zuuroplossing te begrijpen
- Hoe bacteriën mangaanoxide nanodeeltjes produceren

- De efficiëntie van systemen voor het opvangen en omzetten van koolstof verhogen

- Beoordeling van de impact van verliesmechanismen in zonnecelkandidaat-antimoonsulfideselenide

 Luchtkwaliteitsinstanties kunnen gemakkelijker ademen over de huidige emissieregelgeving
Luchtkwaliteitsinstanties kunnen gemakkelijker ademen over de huidige emissieregelgeving Een nieuw zacht magnetisch materiaal kan sneller computergeheugen mogelijk maken
Een nieuw zacht magnetisch materiaal kan sneller computergeheugen mogelijk maken Kleverigheid in glaciale ruimte en tijd
Kleverigheid in glaciale ruimte en tijd  Onderzoekers brengen de wetenschappelijke gemeenschap dichter bij het begrijpen van fusies van dubbelsterren
Onderzoekers brengen de wetenschappelijke gemeenschap dichter bij het begrijpen van fusies van dubbelsterren Hoe ga je in je eigen woorden de volgorde van zuurstof, kooldioxide en bloed omschrijven?
Hoe ga je in je eigen woorden de volgorde van zuurstof, kooldioxide en bloed omschrijven?  Van Canada tot Europa, onderzoek onthult de uitdagingen waarmee vrouwelijke leiders worden geconfronteerd
Van Canada tot Europa, onderzoek onthult de uitdagingen waarmee vrouwelijke leiders worden geconfronteerd  Populariteit van autodeel-apps stimuleert discussie over belastingen
Populariteit van autodeel-apps stimuleert discussie over belastingen Satellietbeelden in uw achtertuin vastleggen en bijdragen aan een momentopname van de klimaatcrisis
Satellietbeelden in uw achtertuin vastleggen en bijdragen aan een momentopname van de klimaatcrisis
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

