
Wetenschap
Entropieverandering bij het oplossen van zout in water?
De entropieverandering voor het oplossen van zout in water kan worden berekend met behulp van de volgende vergelijking:
$$\Delta S =nR\ln(\frac{V_2}{V_1})$$
waar:
* $\Delta S$ is de entropieverandering in J/K
* $n$ is het aantal opgeloste mol zout
* $R$ is de ideale gasconstante (8,314 J/mol K)
* $V_2$ is het volume van de oplossing in L
* $V_1$ is het volume van het water voordat het zout werd opgelost in L
Als bijvoorbeeld 1 mol zout wordt opgelost in 1 liter water, zou de entropieverandering zijn:
$$\Delta S =(1 \text{ mol})(8,314 \text{ J/mol K})\ln(\frac{2 \text{ L}}{1 \text{ L}}) =5,76 \ tekst{ J/K}$$
Deze positieve waarde van $\Delta S$ geeft aan dat de entropie van het systeem toeneemt wanneer zout in water wordt opgelost.
 Van huisdieren tot ongedierte:hoe tamme konijnen de wildernis overleven
Van huisdieren tot ongedierte:hoe tamme konijnen de wildernis overleven  Voorspellers kijken misschien op de verkeerde plaats bij het voorspellen van tornado's, uit onderzoek blijkt
Voorspellers kijken misschien op de verkeerde plaats bij het voorspellen van tornado's, uit onderzoek blijkt Waar haalt het zuidwesten al zijn water vandaan?
Waar haalt het zuidwesten al zijn water vandaan? Hoe overheidsbeleidsmakers gegevens uit nieuw onderzoek kunnen gebruiken om klimaatdoelen te bereiken
Hoe overheidsbeleidsmakers gegevens uit nieuw onderzoek kunnen gebruiken om klimaatdoelen te bereiken  Nieuwe studie laat zien hoe de oude wereld zich aanpaste aan de klimaatverandering
Nieuwe studie laat zien hoe de oude wereld zich aanpaste aan de klimaatverandering
Hoofdlijnen
- Hoe eiwitten hun plaats in de cel vinden
- Schippers dumpen afval in de wateren van Zuid-Florida? Tieners worden beschuldigd van misdrijf
- Onderzoekers ontwikkelen een algoritme om te bepalen hoe cellulaire ‘buurten’ in weefsels functioneren
- Waarom graangewassen beter zijn
- Nieuwe biobronnen voor plantaardige peptidehormonen met behulp van technologie voor het bewerken van genen
- Waar zijn de vrienden van Facebook? Aandelendaling wordt dieper (update)
- Hoe wordt glucose opgeslagen in plantencellen?
- Wetenschappers publiceren nieuw onderzoek naar hoe individuele cellen reageren op virale infecties
- Wat is het verschil tussen een mens en een fruitvlieg?
- Russische wetenschappers ontwikkelden een sensor voor het detecteren van giftige stoffen in waterlichamen

- Nieuw metamateriaal verandert in nieuwe vormen, nieuwe panden aannemen

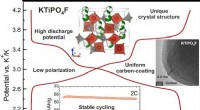
- Wetenschappers ontwikkelen nieuw kathodemateriaal voor metaal-ionbatterijen
- Zoet succes:nieuw enzymatisch biosysteem benut het potentieel van de suikermaltose

- Door licht aangedreven nano-organismen verbruiken CO2, milieuvriendelijke kunststoffen en brandstoffen maken

 NASA kijkt naar Harvey vanuit satellieten en het internationale ruimtestation
NASA kijkt naar Harvey vanuit satellieten en het internationale ruimtestation De 20-minutenbuurt:waarom is het geen belangrijke beleidsrichting?
De 20-minutenbuurt:waarom is het geen belangrijke beleidsrichting? Van bosbranden tot terrorisme:hoe gemeenschappen veerkrachtig worden
Van bosbranden tot terrorisme:hoe gemeenschappen veerkrachtig worden Afbeelding:NASA's Terra-satelliet ziet Cowbell Fire in de Everglades van Florida
Afbeelding:NASA's Terra-satelliet ziet Cowbell Fire in de Everglades van Florida De beginconcentraties berekenen
De beginconcentraties berekenen  Hoe planten de poriën waardoor ze ademen spreiden
Hoe planten de poriën waardoor ze ademen spreiden  Wanneer leerden mensen voor het eerst tellen?
Wanneer leerden mensen voor het eerst tellen?  Studie onderzoekt hoe schone lucht de gemeentelijke obligatiemarkt beïnvloedt
Studie onderzoekt hoe schone lucht de gemeentelijke obligatiemarkt beïnvloedt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

