
Wetenschap
Hoe bepaal je, als je 14,5 mol N2 hebt, hoeveel H2 er theoretisch nodig is om 22,5 NH3 te produceren volgens de reactie plus 3H2 2NH3?
De uitgebalanceerde chemische vergelijking voor de reactie is:
$$N_2 + 3H_2 \pijl naar rechts 2NH_3$$
Uit de stoichiometrie van de reactie kunnen we opmaken dat voor 1 mol N2 3 mol H2 nodig is om 2 mol NH3 te produceren.
Daarom hebben we voor 14,5 mol N2 nodig:
$$14,5 \text{ mol }N_2 \times \frac{3 \text{ mol }H_2}{1 \text{ mol }N_2} =43,5 \text{ mol }H_2$$
Theoretisch zijn er dus 43,5 mol H2 nodig om 22,5 mol NH3 te produceren volgens de gegeven reactie.
 Pulserende aurora:Killer-elektronen in tokkelende luchtlichten
Pulserende aurora:Killer-elektronen in tokkelende luchtlichten Licht werpen op ijzerverrijking in de schemerzone van de oceanen
Licht werpen op ijzerverrijking in de schemerzone van de oceanen Nederlanders onthullen ambitieuze wet om broeikasgassen terug te dringen
Nederlanders onthullen ambitieuze wet om broeikasgassen terug te dringen Wat elk land wel en niet kan doen op Antarctica, in naam van de wetenschap
Wat elk land wel en niet kan doen op Antarctica, in naam van de wetenschap Door smog getroffen Delhi annuleert oneven-even rantsoeneringsplan voor auto's
Door smog getroffen Delhi annuleert oneven-even rantsoeneringsplan voor auto's
Hoofdlijnen
- Pizza-nachtmerries:kan uw dieet uw dromen bepalen?
- Het Bohr-model:snel vervangen maar nooit vergeten
- Zouden mensen bereid zijn hun persoonsgegevens af te staan voor onderzoek?
- Tandwortelpulp wordt een rijke bron van stamcellen
- De definitie van lichaamssystemen
- Soorten berekenen Evenness
- Ziekteverwekkers tegen elkaar keren om resistentie tegen geneesmiddelen te voorkomen
- Kunnen data dolfijnen redden? Hoe wetenschappers NASA-gegevens gebruiken om het verband tussen zonnestormen en het stranden van dieren te bestuderen
- Zaai-tussengezaaide bodembedekkers bieden voordelen voor de V3-maïsoogst
- Synthese van het veterinaire antibioticum florfenicol via een snelle chemo-enzymatische route
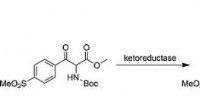
- Hoe seleniumverbindingen katalysatoren kunnen worden

- Bestudeer details waarom 2D-vorming van molybdeendisulfide een snelheidsboost krijgt van zout
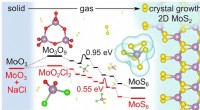
- Turing-structuren in een door mensen gemaakte interface

- Kijken hoe een covalent polymeer zich ontwikkelt met behulp van een scanning tunneling microscoop

 Nikkelferriet bevordert de capaciteit en cyclusstabiliteit van lithium-zwavelbatterijen
Nikkelferriet bevordert de capaciteit en cyclusstabiliteit van lithium-zwavelbatterijen Verschil tussen Engels en metrisch systeem
Verschil tussen Engels en metrisch systeem Drie smaken zijn beter dan één - in ijs- en supernova-onderzoek
Drie smaken zijn beter dan één - in ijs- en supernova-onderzoek Waarom wapenbeheersingswetten niet door het Congres worden aangenomen, ondanks de steun van de meerderheid van het publiek en herhaalde verontwaardiging over massale schietpartijen
Waarom wapenbeheersingswetten niet door het Congres worden aangenomen, ondanks de steun van de meerderheid van het publiek en herhaalde verontwaardiging over massale schietpartijen  Het volume van een massief object meten
Het volume van een massief object meten De onbedoelde gevolgen van het sleutelen aan online prijzen
De onbedoelde gevolgen van het sleutelen aan online prijzen Nieuwe tools volgen actie op klimaatwetten in de staat New York en NYC
Nieuwe tools volgen actie op klimaatwetten in de staat New York en NYC De geschiedenis van de mensheid reconstrueren met behulp van fecale sterolen
De geschiedenis van de mensheid reconstrueren met behulp van fecale sterolen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

